14.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如表:A的气态氢化物能使湿润的红色石蕊试纸变蓝;C单质在实验室一般保存在煤油中;F的最高价氧化物对应水化物既能和酸反应又能和强碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题: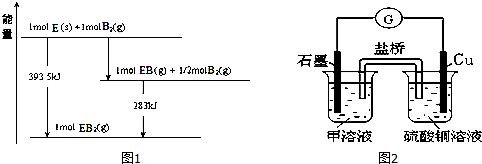
(1)A元素在周期表中的位置是第二周期第VA族.
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)酸雨或光化学烟雾;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若使所得溶液pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.某同学假设正极产物是Fe2+,请你设计实验证明该假设滴加酸性高锰酸钾溶液,若溶液紫色褪去(或滴加铁氰化钾溶液,产生蓝色沉淀),则产品中含有Fe2+.

| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)酸雨或光化学烟雾;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若使所得溶液pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.某同学假设正极产物是Fe2+,请你设计实验证明该假设滴加酸性高锰酸钾溶液,若溶液紫色褪去(或滴加铁氰化钾溶液,产生蓝色沉淀),则产品中含有Fe2+.
13.如表有关实验现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 把SO2通入紫色石蕊试液中 | 紫色褪去 | SO2具有漂白性 |
| B | 确定碳酸氢钠固体中是否含有碳酸钠.把固体溶于水中,加入澄清石灰水 | 有白色沉淀生成 | 碳酸氢钠固体中含有碳酸钠 |
| C | 将NO2球浸泡在热水中 | 红棕色变浅 | 反应2NO2?N2O4的△H<0 |
| D | 向AgCl沉淀中滴加KI溶液 | 白色沉淀变为黄色 | Ksp(AgI)<Ksp (AgCl) |
| A. | A | B. | B | C. | C | D. | D |
12.常温下,下列说法正确的是( )
| A. | 0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) | |
| B. | 等体积、等物质的量浓度的NaCl(aq) 微粒种类大于NaClO(aq)中微粒种类 | |
| C. | pH=3的硫酸溶液中水的电离程度大于pH=11的氨水溶液中水的电离程度 | |
| D. | 体积相同的0.1 mol/L氨水和0.1 mol/L NaOH溶液中和盐酸的能力后者大 |
11.下列说法正确的是( )
| A. | 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 | |
| B. | 铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 | |
| C. | 氢氧燃料电池的能量转换形式之一为化学能转化为电能 | |
| D. | 催化剂通过降低化学反应的焓变加快化学反应速率 |
10.化学中图象可以直观地描述化学反应的进程或结果,如图图象描述正确的是( )


| A. | 图1表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=183kJ•mol-1 | |
| B. | 图2表示室温时用0.1mol•L-1盐酸滴定10mL0.1mol•L-1NaOH溶液,溶液pH随加入酸体积变化 | |
| C. | 图3表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | 图4表示10mL0.1mol/LNa2CO3和NaHCO3两种溶液中,分别滴加0.1mol/LHCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
9.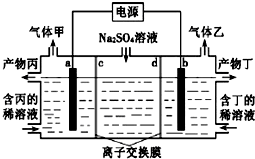 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H2O+2e-═2OH-+H2↑ |
8.下列有关说法正确的是( )
| A. | 加热0.1mol/L Na2CO3溶液时,CO32-的水解程度和溶液的pH均增大 | |
| B. | 100℃时水的离子积常数Kw为5.5×10-13,说明水的电离是放热反应 | |
| C. | 若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 | |
| D. | 0.1 mol•L-1CH3COOH溶液加水稀释后,CH3COOH的电离程度和溶液中C(CH3COO-)的值增大 |
7.下列指定反应的离子方程式正确的是( )
| A. | 实验室用烧碱溶液除去尾气中的Cl2:Cl2+OH-═Cl-+HClO | |
| B. | 稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| C. | 石灰水中加入过量小苏打溶液:2HCO3-+Ca2++2OH-=CaCO3↓+CO32+2H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |
6.如图装置进行相应的实验,能达到实验目的是( )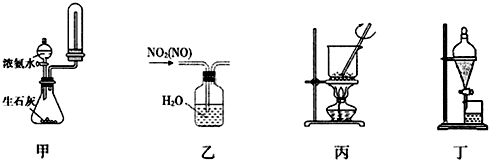

| A. | 用装置甲制取并收集干燥纯净的NH3 | |
| B. | 用装置乙除去NO2中混有的少量NO | |
| C. | 用装置丙将氢氧化钠固体加热熔融 | |
| D. | 用装置丁把溴水中的溴萃取分离出来 |
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
0 173788 173796 173802 173806 173812 173814 173818 173824 173826 173832 173838 173842 173844 173848 173854 173856 173862 173866 173868 173872 173874 173878 173880 173882 173883 173884 173886 173887 173888 173890 173892 173896 173898 173902 173904 173908 173914 173916 173922 173926 173928 173932 173938 173944 173946 173952 173956 173958 173964 173968 173974 173982 203614
| A. | pH=3的溶液中:Na+、NO3-、Fe2+、SO42- | |
| B. | 加入铝粉能产生氢气的溶液中:NH4+、CH3COO-、SO42-、NO3- | |
| C. | 某酸性溶液中Na+、ClO?、SO42?、I? | |
| D. | 在0.1mol•L-1 AlC13溶液中:H+、Na+、Cl-、NO3- |