题目内容
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | pH=3的溶液中:Na+、NO3-、Fe2+、SO42- | |
| B. | 加入铝粉能产生氢气的溶液中:NH4+、CH3COO-、SO42-、NO3- | |
| C. | 某酸性溶液中Na+、ClO?、SO42?、I? | |
| D. | 在0.1mol•L-1 AlC13溶液中:H+、Na+、Cl-、NO3- |
分析 A.pH=3的溶液,显酸性,离子之间发生氧化还原反应;
B.加入铝粉能产生氢气的溶液,为非氧化性酸或强碱溶液;
C.酸性溶液中离子之间发生氧化还原反应;
D.该组离子之间不反应.
解答 解:A.pH=3的溶液,显酸性,H+、NO3-、Fe2+发生氧化还原反应,不能大量共存,故A错误;
B.加入铝粉能产生氢气的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能大量存在NH4+,酸溶液中不能大量存在CH3COO-,故B错误;
C.酸性溶液中ClO?、I?发生氧化还原反应,不能大量共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
15.下列各组离子能在无色强酸性溶液中大量共存的是( )
| A. | Fe3+、Na+、OH-、Cl- | B. | Na+、K+、NO3-、Cl- | ||
| C. | Cu2+、Mg2+、CO32-、Cl- | D. | H+、Na+、MnO4-、SO32- |
16.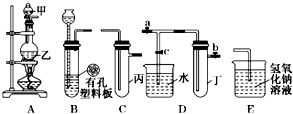 某小组同学用如图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:
某小组同学用如图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:
(1)将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①A中反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;.
②E中氢氧化钠溶液的作用吸收多余的Cl2.
在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论如表:
③.实验Ⅰ推出的相应结论是否合理?不合理,若不合理,请说明理由(若合理,无需填写)没有事先证明干燥的氯气无漂白性.
④.实验Ⅱ推出相应的结论是否合理?不合理,若不合理,请说明理由(若合理,无需填写)制取的氯气中含HCl气体,其溶于水能与NaHCO3粉末反应产生气泡.
(2)将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2并进行有关实验.
①B中反应的化学方程式Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O.
②先若关闭c,当丁中充满红棕色的NO2时,再关闭止水夹a、b,微热试管丁,丁中可观察到的实验现象丁中气体的红棕色变深.
 某小组同学用如图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:
某小组同学用如图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:(1)将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①A中反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;.
②E中氢氧化钠溶液的作用吸收多余的Cl2.
在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论如表:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
④.实验Ⅱ推出相应的结论是否合理?不合理,若不合理,请说明理由(若合理,无需填写)制取的氯气中含HCl气体,其溶于水能与NaHCO3粉末反应产生气泡.
(2)将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2并进行有关实验.
①B中反应的化学方程式Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O.
②先若关闭c,当丁中充满红棕色的NO2时,再关闭止水夹a、b,微热试管丁,丁中可观察到的实验现象丁中气体的红棕色变深.
20.在NaCl饱和溶液中通入HCl(g)时,NaCl(s)能沉淀析出的原因是( )
| A. | HCl水溶液是强酸,任何强酸都导致有沉淀析出 | |
| B. | Cl-浓度增大,使平衡向生成氯化钠的方向移动,生成NaCl(s) | |
| C. | 酸的存在降低了Ksp(NaCl)的数值 | |
| D. | Ksp(NaCl)不受酸的影响,但增加Cl-浓度,能使Ksp(NaCl)减小 |
10.化学中图象可以直观地描述化学反应的进程或结果,如图图象描述正确的是( )
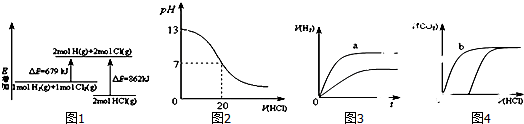

| A. | 图1表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=183kJ•mol-1 | |
| B. | 图2表示室温时用0.1mol•L-1盐酸滴定10mL0.1mol•L-1NaOH溶液,溶液pH随加入酸体积变化 | |
| C. | 图3表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | 图4表示10mL0.1mol/LNa2CO3和NaHCO3两种溶液中,分别滴加0.1mol/LHCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
17.镍是有机合成的重要催化剂.某化工厂有含镍催化剂废品(主要成分是镍,杂质是铁、铝单质及其化合物,少量难溶性杂质).某学习小组设计如图流程利用含镍催化剂废品制备硫酸镍晶体: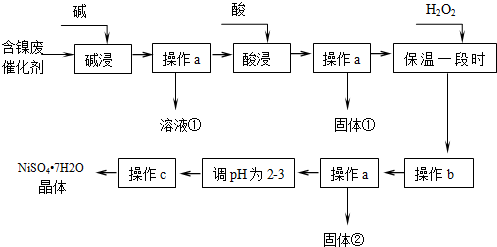
几种难溶碱开始沉淀和完全沉淀的pH如表:
回答下列问题:
(1)溶液①中含金属元素的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O.双氧水可以用下列物质替代的是A.
A.氧气 B.高锰酸钾 C.氯气 D.硝酸
(3)取2.0000g硫酸镍晶体样品溶于蒸馏水,用0.2mol•L-1的EDTA(Na2H2Y)标准溶液滴定至终点,消耗EDTA标准溶液为34.50mL.滴定反应为Ni2++H2Y2-=NiY2-+2H+.计算样品纯度为97.0%.(已知,NiSO4•7H2O相对分子质量为281,不考虑杂质反应).
(4)操作b调节溶液范围为3.2-7.1,其目的是除去Fe3+.固体②的化学式为Fe(OH)3.
(5)操作a和c需要使用的仪器除铁架台(带铁圈)、烧杯、酒精灯、玻璃棒外还需要的主要玻璃仪器是漏斗.上述流程中,“酸浸”时所加入的酸是H2SO4(填化学式).

几种难溶碱开始沉淀和完全沉淀的pH如表:
| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
(1)溶液①中含金属元素的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O.双氧水可以用下列物质替代的是A.
A.氧气 B.高锰酸钾 C.氯气 D.硝酸
(3)取2.0000g硫酸镍晶体样品溶于蒸馏水,用0.2mol•L-1的EDTA(Na2H2Y)标准溶液滴定至终点,消耗EDTA标准溶液为34.50mL.滴定反应为Ni2++H2Y2-=NiY2-+2H+.计算样品纯度为97.0%.(已知,NiSO4•7H2O相对分子质量为281,不考虑杂质反应).
(4)操作b调节溶液范围为3.2-7.1,其目的是除去Fe3+.固体②的化学式为Fe(OH)3.
(5)操作a和c需要使用的仪器除铁架台(带铁圈)、烧杯、酒精灯、玻璃棒外还需要的主要玻璃仪器是漏斗.上述流程中,“酸浸”时所加入的酸是H2SO4(填化学式).
15.某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写实验报告的一部分.
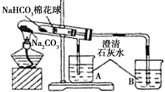
(1)请帮助该小组同学完成实验报告中的内容.
(2)已知:20℃时,Na2CO3的溶解度为20.5g.由实验③(填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5g;如果向饱和Na2CO3溶液中不断通入CO2气体,离子方程式是2Na++CO32-+CO2+H2O═2NaHCO3↓.
(3)用化学方程式说明实验⑥得出结论的原因2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
| 实验序号 | 实验步骤(内容) | 现象 |
| ① | 在贴有标签a、b的试管中分别加入1.0 g Na2CO3固体和NaHCO3固体,观察外观. | / |
| ② | 分别滴入几滴水,振荡,摸试管底部. | 试管 a吸热现象更明显(填“a”或“b”) |
| ③ | 继续向两试管中分别加入10.0 mL水,用力振荡,观察现象. | / |
| ④ | 再分别向两试管中滴加2滴酚酞溶液,观察现象. | 溶液均变红,颜色较深的试管是 a(填“a”或“b”). |
| ⑤ | 最后分别向两溶液中滴加足量盐酸. | 红色褪去,均有无色气体产生.经计算生成气体的是a <b(填“>”“<”或“=”) |
| ⑥ | 加热大试管一段时间.(注:棉花球沾有无水硫酸铜粉末) | / |

(1)请帮助该小组同学完成实验报告中的内容.
(2)已知:20℃时,Na2CO3的溶解度为20.5g.由实验③(填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5g;如果向饱和Na2CO3溶液中不断通入CO2气体,离子方程式是2Na++CO32-+CO2+H2O═2NaHCO3↓.
(3)用化学方程式说明实验⑥得出结论的原因2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.