8.25℃时,某溶液由H2O电离产生的c(H+)=10-13mol•L-1,则下列离子组在该溶液中一定能大量共存的是( )
| A. | Na+、K+、Cl-、SO42- | B. | Na+、HCO3-、SO42-、Cl- | ||
| C. | Fe2+、K+、SO42-、NO3- | D. | K+、NH4+、SO42-、Cl- |
7.稀氨水中存在电离平衡:NH3•H2O?NH4++OH-,若要使平衡正向移动,同时使c(OH-)减小,应加入的物质或采取的措施是( )①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥加入少量MgSO4固体.
| A. | ①②⑤ | B. | ③⑥ | C. | ①②④ | D. | ②④⑤⑥ |
2.H2和I2在一定条件下能发生反应:H2(g)+I2(g)═2HI(g)△H=-a kJ/mol
已知:

下列说法正确的是( )
已知:

下列说法正确的是( )
| A. | H2、I2和HI分子中的化学键都是非极性共价键 | |
| B. | 断开2 mol HI分子中的化学键所需能量约为(c+b+a)kJ | |
| C. | 相同条件下,1molH2(g)和1mol I2(g)总能量小于2mol HI(g)的总能量 | |
| D. | 向密闭容器中加入2mol H2(g)和2mol I2(g),充分反应后放出的热量为2akJ |
1.下列离子或分子能够在指定的分散系中大量共存的是( )
| A. | 铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH${\;}_{4}^{+}$、Cl-、NO${\;}_{3}^{-}$ | |
| B. | 澄清石灰水中:Na+、K+、CH3COO -、HCO${\;}_{3}^{-}$ | |
| C. | c(H+)=10-13mol/L的溶液中:NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、K+、Na+ | |
| D. | 空气中:SO2、NO、N2、NH3 |
20.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.
(1)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(2)A中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液,甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为 .
.
①同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.
③通过实验证明了SCN-中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成NO3-
④SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
0 173485 173493 173499 173503 173509 173511 173515 173521 173523 173529 173535 173539 173541 173545 173551 173553 173559 173563 173565 173569 173571 173575 173577 173579 173580 173581 173583 173584 173585 173587 173589 173593 173595 173599 173601 173605 173611 173613 173619 173623 173625 173629 173635 173641 173643 173649 173653 173655 173661 173665 173671 173679 203614
| 操 作 | 现 象 |
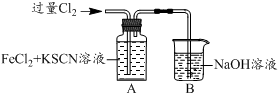 | I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液,甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
 .
.①同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.
③通过实验证明了SCN-中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成NO3-
④SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.


 ),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N原子在同一周期(或电子层数相同),N原子核电荷数更大,原子半径更小,原子核对外层电子的吸引力更强.
),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N原子在同一周期(或电子层数相同),N原子核电荷数更大,原子半径更小,原子核对外层电子的吸引力更强. .
.
 ;NH3的稳定性比PH3强(填写“强”或“弱”).
;NH3的稳定性比PH3强(填写“强”或“弱”).
 NH3•H2O
NH3•H2O NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;.
NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;.