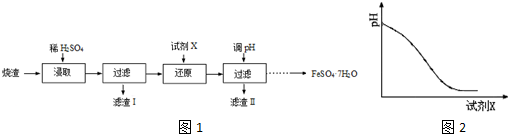
14.已知草酸镍晶体(NiC2O4•2H2O)难溶于水,工业上从废镍催化剂(成分主要为Ni,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:

已知:①相关金属离子生成氢氧化物沉淀的pH如表:
②Ksp(CaF2)=1.46×10-10
③当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)pH的调控范围为5.0≤pH<6.8.
(4)写出“沉镍”时反应的离子方程式Ni2++C2O42-+2H2O=NiC2O4•2H2O,当Ca2+沉淀完全时,溶液中c(F-)>$\sqrt{\frac{1.46×10{\;}^{-10}}{10{\;}^{-5}}}$mol•L-1(写出计算式即可).

已知:①相关金属离子生成氢氧化物沉淀的pH如表:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的PH | 3.2 | 8.8 | 5.0 | 9.5 |
③当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)pH的调控范围为5.0≤pH<6.8.
(4)写出“沉镍”时反应的离子方程式Ni2++C2O42-+2H2O=NiC2O4•2H2O,当Ca2+沉淀完全时,溶液中c(F-)>$\sqrt{\frac{1.46×10{\;}^{-10}}{10{\;}^{-5}}}$mol•L-1(写出计算式即可).
10. 碳及其含碳化合物在人们的生产生活中应用广泛.
碳及其含碳化合物在人们的生产生活中应用广泛.
(1)将不同量的CO2(g)和H2(g)分别通入到体积为2L的恒容密闭容器中,进行反应2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),得到如表三组数据;
①实验1中以v(H2)表示的反应速率为0.4mol/(L.min)
②900℃化学平衡常数为0.12,第3组与第2组相比CO2的转化率增大(填“增大”“减小”“不变”不能确定).
(2)将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒).持续通入甲烷,在标准状况下,消耗甲烷体积VL.
①0<V≤44.8L时,电池总反应方程式为CH4+2O2+2KOH=K2CO3+3H2O
②44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-
③V=67.2L时,溶液中离子浓度大小关系为c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
0 173484 173492 173498 173502 173508 173510 173514 173520 173522 173528 173534 173538 173540 173544 173550 173552 173558 173562 173564 173568 173570 173574 173576 173578 173579 173580 173582 173583 173584 173586 173588 173592 173594 173598 173600 173604 173610 173612 173618 173622 173624 173628 173634 173640 173642 173648 173652 173654 173660 173664 173670 173678 203614
 碳及其含碳化合物在人们的生产生活中应用广泛.
碳及其含碳化合物在人们的生产生活中应用广泛.(1)将不同量的CO2(g)和H2(g)分别通入到体积为2L的恒容密闭容器中,进行反应2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),得到如表三组数据;
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 时间/min | ||
| CO2 | H2 | H2 | C2H5OH | |||
| 1 | 650 | 2 | 6.8 | 2.0 | 0.8 | 6 |
| 2 | 900 | 2 | 4.4 | 2.0 | 0.4 | 3 |
| 3 | 900 | 4 | 8.8 | C | d | t |
②900℃化学平衡常数为0.12,第3组与第2组相比CO2的转化率增大(填“增大”“减小”“不变”不能确定).
(2)将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒).持续通入甲烷,在标准状况下,消耗甲烷体积VL.
①0<V≤44.8L时,电池总反应方程式为CH4+2O2+2KOH=K2CO3+3H2O
②44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-
③V=67.2L时,溶液中离子浓度大小关系为c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
 .
.