7.有关元素X、Y、Z、D、E的信息如下
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法不正确的是②③(填序号).
①保存EY2溶液时,需向溶液加入少量E单质.
②通常实验室配制EY3溶液时,直接用水溶解EY3固体即可.
③EY2只能通过置换反应生成,EY3只能通过化合反应生成.
④铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒.
(3)用化学符号表示D2Z的水溶液中各离子浓度从大到小的顺序是Na+>S2->OH->HS->H+.
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm. |
| Y | 所在主族序数与所在周期序数之差为4. |
| Z | 原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰. |
| D | 最高价氧化物对应的水化物,能电离出离子数、电子数都相等的阴、阳离子. |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏. |
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法不正确的是②③(填序号).
①保存EY2溶液时,需向溶液加入少量E单质.
②通常实验室配制EY3溶液时,直接用水溶解EY3固体即可.
③EY2只能通过置换反应生成,EY3只能通过化合反应生成.
④铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒.
(3)用化学符号表示D2Z的水溶液中各离子浓度从大到小的顺序是Na+>S2->OH->HS->H+.
6.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 大量排放氮氧化物可以形成酸雨、产生光化学烟雾,威胁人类生活环境 | |
| B. | 食用地沟油对人体危害大,但地沟油可用来制肥皂 | |
| C. | 明矾水解可生成Al(OH)3胶体,常用于水的杀菌消毒 | |
| D. | 人们可利用元素周期律在过渡元素中寻找性能优良的催化剂 |
4.电镀等工业废水中常含有剧毒、致癌的Cr2O72-.该废水处理的一种方法是:利用还原剂把Cr2O72-还原成毒性较低的Cr3+,再加碱生成沉淀.另一种方法是:向废水中加入适当的NaCl,用Fe作电极进行电解.下列说法错误的是( )
| A. | 电解时,阳极反应为:Fe-2e-=Fe2+ | |
| B. | 电解过程中阴极能产生氢气 | |
| C. | 电解过程中,Cr2O72-在阳极放电 | |
| D. | 电解过程中,溶液中生成Cr(OH)3和Fe(OH)3沉淀 |
3.钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染.
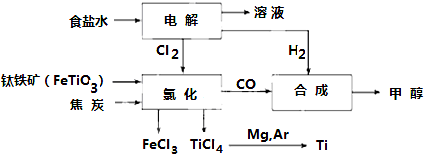
请回答下列问题:
(1)Fe位于元素周期表中第四周期第VIII族.
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2•xH2O,再经焙烧制得.写出TiCl4水解的化学方程式:TiCl4+(2+x)H2O=TiO2.xH2O↓+4HCl.
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
(5)电解食盐水的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.

请回答下列问题:
(1)Fe位于元素周期表中第四周期第VIII族.
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2•xH2O,再经焙烧制得.写出TiCl4水解的化学方程式:TiCl4+(2+x)H2O=TiO2.xH2O↓+4HCl.
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
2.通过火法冶金炼出的铜是粗铜,含有Zn、Fe、Ag、Au等杂质.在实验室条件下用CuSO4溶液作电解液进行电解精炼,并对电解废液进行综合处理.
(1)电解精炼铜时粗铜板作阳极,阴极电极反应式为Cu2++2e-═Cu.电解过程中,电解液中c(Cu2+)变小(填变大、变小、不变).对电解废液进行如下处理

已知:①某些金属离子形成氢氧化物沉淀的pH如表
②Zn(OH)2+2NaOH=Na2ZnO2+2H2O
(2)滤液l中加入H2O2发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加NaOH溶液调节溶液pH的范围是3.2≤pH<4.7.
(4)滤渣1跟稀HNO3反应的化学方程式是3Ag+4HNO3═3AgNO3+NO↑+2H2O.
(1)电解精炼铜时粗铜板作阳极,阴极电极反应式为Cu2++2e-═Cu.电解过程中,电解液中c(Cu2+)变小(填变大、变小、不变).对电解废液进行如下处理

已知:①某些金属离子形成氢氧化物沉淀的pH如表
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 4.7 | 5.4 |
| 完全沉淀 | 3.2 | 9.7 | 6.7 | 8.0 |
(2)滤液l中加入H2O2发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加NaOH溶液调节溶液pH的范围是3.2≤pH<4.7.
(4)滤渣1跟稀HNO3反应的化学方程式是3Ag+4HNO3═3AgNO3+NO↑+2H2O.
20.下列指定反应的离子方程式正确的是( )
| A. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | Cu溶于稀HNO3:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
19.向甲溶液中缓慢滴加乙溶液,反应生成沉淀的质量与乙溶液的量之间的关系如图所示,其中符合图象的是( )
0 173473 173481 173487 173491 173497 173499 173503 173509 173511 173517 173523 173527 173529 173533 173539 173541 173547 173551 173553 173557 173559 173563 173565 173567 173568 173569 173571 173572 173573 173575 173577 173581 173583 173587 173589 173593 173599 173601 173607 173611 173613 173617 173623 173629 173631 173637 173641 173643 173649 173653 173659 173667 203614
| 甲 | 乙 | 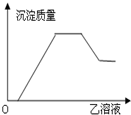 | |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH | |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 | |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH | |
| D | NaAlO2、氨水、NaOH | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
 已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系:
