6.海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程.下列有关说法正确的是( )

| A. | 用澄清的石灰水可鉴别NaHCO3和Na2CO3 | |
| B. | Na2CO3的热稳定性大于NaHCO3 | |
| C. | 在第③、④、⑤步骤中,溴元素均被氧化 | |
| D. | 工业上通过电解饱和MgCl2溶液制取金属镁 |
5.下表是元素周期表一部分,针对表中①~⑩种元素,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与④最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(3 )⑨最高价氧化物的水化物电子式是 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.
(4)表中最高价氧化物的水化物中,酸性最强的是HClO4(填化学式)
(5)③元素与⑩元素两者核电荷数之差是26.
(6)在⑦与⑩的单质中,化学性质较活泼的物质名称是氯气,可用什么化学反应说明该事实(写出反应的离子方程式):Cl2+2Br-=2Cl-+Br2.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与④最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(3 )⑨最高价氧化物的水化物电子式是
 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.(4)表中最高价氧化物的水化物中,酸性最强的是HClO4(填化学式)
(5)③元素与⑩元素两者核电荷数之差是26.
(6)在⑦与⑩的单质中,化学性质较活泼的物质名称是氯气,可用什么化学反应说明该事实(写出反应的离子方程式):Cl2+2Br-=2Cl-+Br2.
4.如表是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,B元素的原子核内质子数等于中子数.
(1)写出A、B、C三种元素符号:P、O、Cl
(2)B元素位于周期表中第二周期第ⅥA族
(3)C的气态氢化物水溶液显酸性(填“酸”或“碱”)
| B | ||
| A | C |
(2)B元素位于周期表中第二周期第ⅥA族
(3)C的气态氢化物水溶液显酸性(填“酸”或“碱”)
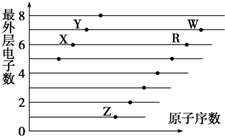
3.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法不正确的是( )

| A. | X和R在同一主族 | |
| B. | 含氧酸酸性:W>R | |
| C. | X与W可以形成酸性氧化物 | |
| D. | X、Z形成的化合物中可能含有共价键 |
2. 短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )
短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )
 短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )
短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )| A. | x与同主族且相邻元素的气态氢化物的沸点,前者高于后者 | |
| B. | 含Y元素的盐溶液有的显酸性,有的显碱性 | |
| C. | x的气态氢化物与w的最高价氧化物的水化物反应只能生成一种盐 | |
| D. | x与H、O元素形成的化合物可以组成一种盐,其中X.H.O元素原子个数之比为2:4:3 |
1.四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法不正确的是( )

0 173052 173060 173066 173070 173076 173078 173082 173088 173090 173096 173102 173106 173108 173112 173118 173120 173126 173130 173132 173136 173138 173142 173144 173146 173147 173148 173150 173151 173152 173154 173156 173160 173162 173166 173168 173172 173178 173180 173186 173190 173192 173196 173202 173208 173210 173216 173220 173222 173228 173232 173238 173246 203614

| A. | 元素形成的简单离子的半径Z<M | |
| B. | Y的最高价氧化物对应水化物的酸性比X 的强 | |
| C. | X 的最简单气态氢化物的热稳定性比Z的小 | |
| D. | Z位于元素周期表中第2 周期、第ⅥA族 |
 生物柴油是高级脂肪酸甲酯,可由油脂与甲醇通过取代反应(酯交换,生成新酯和新醇)得到,用菜籽油制备生物柴油的步骤如下:
生物柴油是高级脂肪酸甲酯,可由油脂与甲醇通过取代反应(酯交换,生成新酯和新醇)得到,用菜籽油制备生物柴油的步骤如下: 某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管B中放入铁粉和石棉绒的混合物,再结合一些步骤,就可以完成髙温下“Fe与水蒸气的反应实验”(己知石棉绒是耐高温材料,不与水和铁反应).
某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管B中放入铁粉和石棉绒的混合物,再结合一些步骤,就可以完成髙温下“Fe与水蒸气的反应实验”(己知石棉绒是耐高温材料,不与水和铁反应). 红磷P(s)和Cl2(g)发生反应生成PCl3(g),继续反应生成PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).
红磷P(s)和Cl2(g)发生反应生成PCl3(g),继续反应生成PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).