0 17196 17204 17210 17214 17220 17222 17226 17232 17234 17240 17246 17250 17252 17256 17262 17264 17270 17274 17276 17280 17282 17286 17288 17290 17291 17292 17294 17295 17296 17298 17300 17304 17306 17310 17312 17316 17322 17324 17330 17334 17336 17340 17346 17352 17354 17360 17364 17366 17372 17376 17382 17390 203614



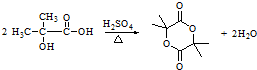

 +NaOH
+NaOH +NaCl+H2O
+NaCl+H2O
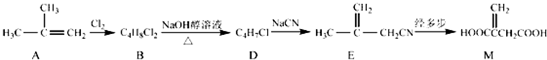
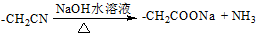 ,E经五步转成变成M的合成反应流程为:
,E经五步转成变成M的合成反应流程为: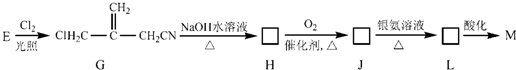

 +NaCl+NH3
+NaCl+NH3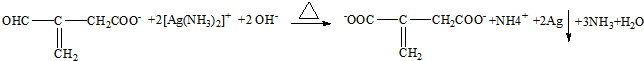
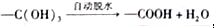 ,E经三步转变成M的合成反应流程为
,E经三步转变成M的合成反应流程为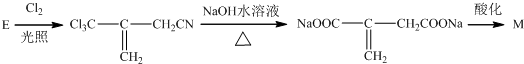
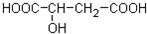 近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构简式如图所示.请按要求回答问题:
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构简式如图所示.请按要求回答问题:



 名称是
名称是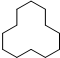 名称为
名称为 )的官能团的名称:
)的官能团的名称: 图是一个正方体,设想将一个甲烷分子放入,碳原子将位于该正方体的中心,黑球表示已有一个氢原子属该正方体的一角.请在图中另画三个黑球表示其他3个氢原子的位置
图是一个正方体,设想将一个甲烷分子放入,碳原子将位于该正方体的中心,黑球表示已有一个氢原子属该正方体的一角.请在图中另画三个黑球表示其他3个氢原子的位置