20.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为原来的60%,则( )
| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率增大了 | ||
| C. | 物质B的质量分数减小了 | D. | a>b |
19.工业上可利用合成气(CO和H2的混合气体)生产甲醇.已知:CO(g)+2H2(g)?CH3OH(g)△H=-92.9kJ/mol.一定条件下,该反应在一体积固定的密闭容器中达到平衡.下列说法正确的是( )
| A. | 该反应的△S>0 | |
| B. | 该反应在任何温度下均能自发进行 | |
| C. | 向容器中充入少量He,平衡向正反应方向移动 | |
| D. | 升高温度平衡向逆反应方向移动 |
18.下列事实中不能应用勒夏特列原理来解释的是( )
| A. | 新制的氯水在光照条件下颜色变浅 | |
| B. | 高压对合成氨有利 | |
| C. | 将NO2和N2O4的混合气体降温后,气体颜色变浅 | |
| D. | 加入催化剂能使合成氨的速率加快 |
17.一定温度下,在固定体积的密闭容器中进行下列反应
4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 若单位时间内生成xmolNO的同时消耗x molNH3,则反应达到平衡状态 | |
| B. | 当混合气体的压强不再改变,则说明反应已达到平衡状态 | |
| C. | 当混合气体的密度不再改变,则说明反应已达到平衡状态 | |
| D. | 达到化学平衡后,若增大容器容积,正反应速率减小,逆反应速率增大 |
16. 如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
 如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )| A. | X的平衡转化率为85% | |
| B. | 第6 min 后,反应就终止了 | |
| C. | 若升高温度,X的平衡转化率将大于85% | |
| D. | 若降低温度,v正减小,v逆增大 |
15.已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,将1mol N2和3mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量(忽略能量损失)( )
| A. | 一定大于92.4 kJ | B. | 一定小于92.4 kJ | C. | 一定等于92.4 kJ | D. | 无法确定 |
14.下列关于反应能量的说法正确的是( )
0 172540 172548 172554 172558 172564 172566 172570 172576 172578 172584 172590 172594 172596 172600 172606 172608 172614 172618 172620 172624 172626 172630 172632 172634 172635 172636 172638 172639 172640 172642 172644 172648 172650 172654 172656 172660 172666 172668 172674 172678 172680 172684 172690 172696 172698 172704 172708 172710 172716 172720 172726 172734 203614
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ•mol-1,则反应物总能量大于生成物总能量 | |
| B. | 相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则含1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量 |
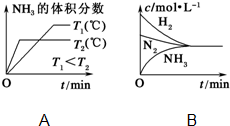 已知工业上合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,回答以下问题:
已知工业上合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,回答以下问题: 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察下图,然后回答问题:
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察下图,然后回答问题: