3.在硫化氢的水溶液中,存在以下平衡:H2S═HS-H+、HS-═H++S2-,若使溶液的pH减小,则c(S2-)( )
| A. | 增大 | B. | 减小 | ||
| C. | 不变 | D. | 可能增大也可能减小 |
2.甲醇是重要的化工原料,又可称为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H1
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)═CO(g)+H2O(g)△H3
回答下列问题:
已知反应①中的相关的化学键键能数据如下:
由此计算△H1=___kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3=___kJ.mol-1( )
①CO(g)+2H2(g)═CH3OH(g)△H1
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)═CO(g)+H2O(g)△H3
回答下列问题:
| 化学键 | H-H | C-O | C O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=___kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3=___kJ.mol-1( )
| A. | 99、-41 | B. | +99、+41 | C. | -99、+41 | D. | -99、41 |
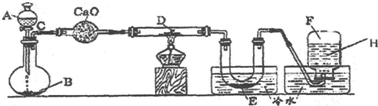
1.下列各图所示的实验原理、方法、装置或操作,其中正确的是( )
| A. |  向容量瓶中转移溶液 | B. |  中和热的测定 | ||
| C. |  浓硫酸与铜的反应 | D. |  乙二酸晶体受热分解 |
20.将2.4g Fe、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g.则收集到的气体体积V的值不可能为( )
| A. | 1.02 | B. | 1.68 | C. | 1.00 | D. | 0.986 |
19.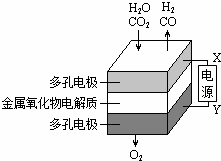 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ=H2+O2ˉ | |
| C. | 总反应可表示为:H2O+CO2=H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
18.某氖原子的质量是a g,12C原子的质量是bg用NA表示阿伏加德罗常数,则以下叙述中错误的是( )
0 172538 172546 172552 172556 172562 172564 172568 172574 172576 172582 172588 172592 172594 172598 172604 172606 172612 172616 172618 172622 172624 172628 172630 172632 172633 172634 172636 172637 172638 172640 172642 172646 172648 172652 172654 172658 172664 172666 172672 172676 172678 172682 172688 172694 172696 172702 172706 172708 172714 172718 172724 172732 203614
| A. | 该氖原子的相对原子质量为12a/b | |
| B. | Wg该氖原子的物质的量为W/aNA mol | |
| C. | Wg 该氖原子所含的质子数为 10W/a个 | |
| D. | 氖元素的摩尔质量为aNA g/mol |

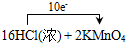 ═2KCl+2MnCl2+5Cl2↑+8H2O
═2KCl+2MnCl2+5Cl2↑+8H2O