11.实验室中需要配制1mol/L的NaCl溶液970mL,配制时应选用的容量瓶的规格是( )
| A. | 950mL 容量瓶 | B. | 500mL容量瓶 | ||
| C. | 1000mL 容量瓶 | D. | 任意规格的容量瓶 |
10.在一定条件下,科学家利用从烟道气中分离出的CO2与太阳能电池电解水产生的H2合成甲醇,其过程如图所示,试回答下列问题:

(1)该合成路线对于环境保护的价值在于减少烟道气中二氧化碳排放到空气中造成温室效应.
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-;.
(3)CH3OH(l)、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:CO2(g)+3H2(g)═CH3OH(l)+H2O(l)△H=-131.9KJ/mol.
(4)据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇也已成为现实.
2CO2(g)+6H2(g),CH3CH2OH(g)+3H2O(g);下列叙述正确的是acd.
a.使用催化剂可能大大提高生产效率
b.反应需在300℃进行可推测该反应是吸热反应
c.充入过量CO2气体可提高H2的转化率
d.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
(5)在一定体积的密闭容器中,CO2和H2也可以进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),
其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
①该反应为吸热反应(填“吸热”或“放热”).
②能判断该反应达到化学平衡状态的依据是BC.
A.容器中压强不变 B.混合气体中c(CO)不变 C.v(H2)正=v(H2O)逆
D.c(CO)=c(H2) E.混合气体的密度保持不变 F.混合气体的平均相对分子质量保持不变
③在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol/L,c(H2)为 1.5mol/L,c(CO) 为 1mol/L,c(H2O) 为 3mol/L,则下一时刻,反应向逆向移动(填“正向”“逆向”或“不”).

(1)该合成路线对于环境保护的价值在于减少烟道气中二氧化碳排放到空气中造成温室效应.
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-;.
(3)CH3OH(l)、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:CO2(g)+3H2(g)═CH3OH(l)+H2O(l)△H=-131.9KJ/mol.
(4)据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇也已成为现实.
2CO2(g)+6H2(g),CH3CH2OH(g)+3H2O(g);下列叙述正确的是acd.
a.使用催化剂可能大大提高生产效率
b.反应需在300℃进行可推测该反应是吸热反应
c.充入过量CO2气体可提高H2的转化率
d.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
(5)在一定体积的密闭容器中,CO2和H2也可以进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),
其化学平衡常数K和温度T的关系如表所示:
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应为吸热反应(填“吸热”或“放热”).
②能判断该反应达到化学平衡状态的依据是BC.
A.容器中压强不变 B.混合气体中c(CO)不变 C.v(H2)正=v(H2O)逆
D.c(CO)=c(H2) E.混合气体的密度保持不变 F.混合气体的平均相对分子质量保持不变
③在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol/L,c(H2)为 1.5mol/L,c(CO) 为 1mol/L,c(H2O) 为 3mol/L,则下一时刻,反应向逆向移动(填“正向”“逆向”或“不”).
9.下列叙述正确的是( )
| A. | 0.1 mol•L-1的硫酸铵溶液中:c(SO42->c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1 mol•L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 1.0×l0-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 | |
| D. | 常温下,1mLpH=1的盐酸与l00mL pH=11的NaOH溶液混合后,溶液的pH=7 |
8.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| ① | 由水电离的c(H+)=l×l0-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| ② | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | |
| ③ | Kw/c(H+)=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- | |
| ④ | FeCl2溶液:K+、Na+、SO42-、AlO2- |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
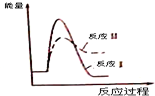
5.如图所示与对应的叙述相符的是( )

0 172387 172395 172401 172405 172411 172413 172417 172423 172425 172431 172437 172441 172443 172447 172453 172455 172461 172465 172467 172471 172473 172477 172479 172481 172482 172483 172485 172486 172487 172489 172491 172495 172497 172501 172503 172507 172513 172515 172521 172525 172527 172531 172537 172543 172545 172551 172555 172557 172563 172567 172573 172581 203614

| A. | 图甲表示使用催化剂后,该反应的△H变小 | |
| B. | 图乙表示反应NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.4kJ•mol-1反应的平衡常数随温度的变化 | |
| C. | 图丙表示反应H2(g)+I2(g)?2HI(g)中H2的转化率随压强的变化 | |
| D. | 图丁表示在饱和Na2SO4溶液中逐步加BaCO3固体后,溶液中c(${SO}_{4}^{2-}$)的浓度变化 |



 某化学实验小组对钠与水的反应进行了研究,他们设计了如图所示的实验装置.请回答下列问题:
某化学实验小组对钠与水的反应进行了研究,他们设计了如图所示的实验装置.请回答下列问题: