20.溴、碘主要存在于海水中,有“海洋元素”的美称,海水中的碘富集在海藻中,我国海带产量局世界第一,除供食用外,大量用于制碘,提取碘的途径如下所示:
干海带$\stackrel{焙烧}{→}$海带灰$\stackrel{水}{→}$水溶液$\stackrel{氧化}{→}$$\stackrel{A}{→}$$\stackrel{B}{→}$→碘单质
下列有关叙述不正确的是( )
干海带$\stackrel{焙烧}{→}$海带灰$\stackrel{水}{→}$水溶液$\stackrel{氧化}{→}$$\stackrel{A}{→}$$\stackrel{B}{→}$→碘单质
下列有关叙述不正确的是( )
| A. | 碘元素在海水中没有游离态存在 | |
| B. | 在提取的过程中用的氧化剂可以是H2O2 | |
| C. | 操作A是萃取 | |
| D. | B是提纯操作,常用蒸馏 |
19.为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W0g样品进行实验,下列实验方法所对应的实验方案和测量数据合理(除w0外)( )
| 实验方法 | 实验方案 | 测量数据 | |
| A. | 量气法 | 将样品与盐酸反应,气体通过排水量气装置量气 | 排水体积 |
| B. | 量气法 | 将样品与盐酸反应,生成的气体全部被碱石灰吸收 | 碱石灰增重 |
| C. | 重量法 | 样品放入烧瓶中,置于电子天平上,加入足量盐酸 | 减轻的质量 |
| D. | 滴定法 | 将样品配成100mL溶液,取10mL加入酚酞,用标准盐酸确定 | 消耗盐酸的体积 |
| A. | A | B. | B | C. | C | D. | D |
16.已知25℃时:
①HF(aq)+OH-(aq)?F-(aq)+H2O(1)△H=-67.7kJ/mol
②H+(aq)+OH-(aq)═H2O(1)△H=-57.3kJ/mol
下列有关说法中正确的是( )
①HF(aq)+OH-(aq)?F-(aq)+H2O(1)△H=-67.7kJ/mol
②H+(aq)+OH-(aq)═H2O(1)△H=-57.3kJ/mol
下列有关说法中正确的是( )
| A. | HF电离吸热 | |
| B. | 水解消耗0.1 mol F时,吸收的热量为6.77 kJ | |
| C. | 中和热均为57.3 kJ/mol | |
| D. | 含0.1 mol HF、0.1 mol NaOH的两种溶液混合后放出的热量为6.77 kJ |
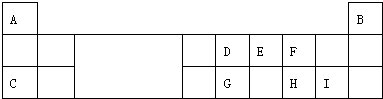
15.下表为元素周期表的一部分,请回答有关问题:
(1)①和⑤的元素符号是N和Si.
(2)表中最活泼的金属是K,非金属性最强的元素是F.(填写元素符号)
(3)表中能形成两性氢氧化物的元素是Al(填写元素符号),分别写出该元素的氢氧化物与⑥⑨最高价氧化物的水化物反应的化学方程式:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O,Al(OH)3+KOH=KAlO2+2H2O.
(4)⑦和⑩元素形成单质的氧化性的强弱为Cl2>Br2.(用化学符号表示)证明该结论的一个实验事实(用离子方程式表示)Cl2+2Br-=2Cl-+Br2.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是K,非金属性最强的元素是F.(填写元素符号)
(3)表中能形成两性氢氧化物的元素是Al(填写元素符号),分别写出该元素的氢氧化物与⑥⑨最高价氧化物的水化物反应的化学方程式:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O,Al(OH)3+KOH=KAlO2+2H2O.
(4)⑦和⑩元素形成单质的氧化性的强弱为Cl2>Br2.(用化学符号表示)证明该结论的一个实验事实(用离子方程式表示)Cl2+2Br-=2Cl-+Br2.
14.L、M、R、T、W是原子序数依次增大的短周期元素,M、T在周期表中的相对位置如表,L与R原子的最外层电子数相同,R的单质是一种常见的半导体材料;M和T的氧化物是常见的引起酸雨的大气污染物.请回答下列问题:
(1)T离子的结构示意图 ;元素W在周期表中的位置是第三周期第ⅦA族.
;元素W在周期表中的位置是第三周期第ⅦA族.
M的气态氢化物与最高价氧化物的水化物能形成一种离子化合物,该离子化合物的化学式为NH4NO3.
(2)在加热条件下,L的单质与T的最高价氧化物的水化物的浓溶液反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
L的单质能置换出R的单质,请写出对应的方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
(3)下列有关相应元素非金属性强弱比较的说法正确的是AC(填字母)
A.M的气态氢化物比R的气态氢化物稳定,则非金属性M强于R
B.高温下,L的单质能从R的最高价氧化物中置换出R,则非金属性L强于R
C.W的核电荷数比T多,原子半径比T小,得电子能力强,则非金属性W强于T.
0 171982 171990 171996 172000 172006 172008 172012 172018 172020 172026 172032 172036 172038 172042 172048 172050 172056 172060 172062 172066 172068 172072 172074 172076 172077 172078 172080 172081 172082 172084 172086 172090 172092 172096 172098 172102 172108 172110 172116 172120 172122 172126 172132 172138 172140 172146 172150 172152 172158 172162 172168 172176 203614
| M | |
| T |
 ;元素W在周期表中的位置是第三周期第ⅦA族.
;元素W在周期表中的位置是第三周期第ⅦA族.M的气态氢化物与最高价氧化物的水化物能形成一种离子化合物,该离子化合物的化学式为NH4NO3.
(2)在加热条件下,L的单质与T的最高价氧化物的水化物的浓溶液反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
L的单质能置换出R的单质,请写出对应的方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
(3)下列有关相应元素非金属性强弱比较的说法正确的是AC(填字母)
A.M的气态氢化物比R的气态氢化物稳定,则非金属性M强于R
B.高温下,L的单质能从R的最高价氧化物中置换出R,则非金属性L强于R
C.W的核电荷数比T多,原子半径比T小,得电子能力强,则非金属性W强于T.
 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”). .
.
 .
.