6.一定条件下,建立平衡2NO2(g)?N2O4(g),以下说法正确的是( )
| A. | 恒温恒容,再充入NO2,达到新平衡时,NO2的体积分数增大 | |
| B. | 恒温恒容,再充入N2,达到新平衡时,容器内颜色变浅 | |
| C. | 恒温恒容,再充入N2O4,达到新平衡时,混合气体的平均相对分子质量增大 | |
| D. | 恒温恒压,再充入Ar,达到新平衡时,NO2的转化率降低 |
5.已知:氨水的密度为0.990g/cm3时,NH3的质量分数为20%;氨水的密度为0.930g/cm3时,NH3的质量分数为18%.质量分数分别为a%和5a%的氨水按等体积混合均匀后,混合溶液中NH3的质量分数为( )
| A. | 3a% | B. | 6a% | C. | 大于3a% | D. | 小于3a% |
4.中和热测定实验中,下列操作一定会降低实验准确性的是( )
| A. | 用滴定管取所用药品 | |
| B. | NaOH溶液在倒入小烧杯时,有少量溅出 | |
| C. | 大小烧杯体积相差较大,夹层间放的碎泡沫塑料较多 | |
| D. | 测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度 |
3.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol.下列结论正确的是( )
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=-57.3kJ/mol.下列结论正确的是( )
| A. | 碳的燃烧热小于110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出的热量小于57.3 kJ |
1.已知某元素的+2价离子的电子排布式为1s22s22p63s23p6,则该元素在周期表中的位置正确的是( )
| A. | 第三周期ⅣA族,p区 | B. | 第四周期ⅡA族,s区 | ||
| C. | 第四周期Ⅷ族,d区 | D. | 第四周期ⅡB族,s区 |
20.下列表示有机化合物分子的方法中不正确的是( )
| A. | 3甲基5庚烯: | B. | 异戊烷: | ||
| C. | 乙酸乙酯:CH3COOCH2CH3 | D. | 甲烷: |
19.下列说法中正确的是( )
| A. | 3p2表示3p能级有两个轨道 | |
| B. | M能层中的原子轨道数目为3 | |
| C. | 1s22s12p1表示的是激发态原子的电子排布 | |
| D. | 处于同一轨道上的电子可以有多个,它的运动状态完全相同 |
18.在光照条件下,将1molCH4与Cl2反应,得到等物质的量的4种取代物,则耗Cl2物质的量为( )
| A. | 1mol | B. | 2mol | C. | 2.5mol | D. | 10mol |
17.水溶液中的Xn+、Ym+、Zn-三种离子,已知m>n,且X、Y、Z三种原子的M层电子数均为奇数.下列说法中不正确的是( )
0 171837 171845 171851 171855 171861 171863 171867 171873 171875 171881 171887 171891 171893 171897 171903 171905 171911 171915 171917 171921 171923 171927 171929 171931 171932 171933 171935 171936 171937 171939 171941 171945 171947 171951 171953 171957 171963 171965 171971 171975 171977 171981 171987 171993 171995 172001 172005 172007 172013 172017 172023 172031 203614
| A. | 三种元素的最高正价氧化物的相应水化物之间能两两反应 | |
| B. | Ym+的半径最小 | |
| C. | Y元素一定是金属元素 | |
| D. | 原子半径:Z>X>Y |

 →
→
 ,其核磁共振氢谱有2种峰.
,其核磁共振氢谱有2种峰. ,
,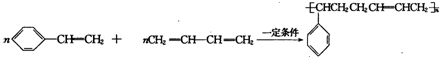 .
. (其中一种).
(其中一种).