12.下列四组混合气体(体积比)为①NO2:O2=1:1 ②NO:O2=1:1 ③NH3:O2=1:1④NO2:NO:O2=1:1:1,将分别盛满上述各种气体的容积相等的四支试管倒置于盛有水的水槽中,最后试管内液面由低到高顺序正确的是( )
| A. | ④③②① | B. | ④①②③ | C. | ①③②④ | D. | ③①②④ |
11.a、b、c、d、e 是同周期的五种主族元素,五种元素的原子得失电子后所形成的简单离子中,e的离子半径最小,c 和 d的最高价氧化物的水化物显酸性且酸性c>d,a 和 b形成阳离子的氧化性a>b,e为金属元素.则它们的原子序数由小到大的顺序是( )
| A. | baedc | B. | edabc | C. | abdce | D. | ebadc |
10.I.某化学课外活动小组对污染大气的部分非金属氧化物进行探究.请根据题目要求回答下列问题.

(1)写出用硝酸制取一氧化氮的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(2)查资料得知,HCOOH$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+H2O.实验室有如图1所示的装置,制取CO气体可选用的装置为A(填序号),实验室利用该装置还可制取的常见气体有Cl2(填写一种气体的分子式).
(3)查资料得知,利用催化剂可使汽车尾气中的一氧化碳和氮氧化物大部分发生反应转化为二氧化碳和氮气.该小组在实验室模拟汽车尾气处理,设计了如图2所示装置(部分夹持和装置已略去).
①实验前关闭旋塞K,先通氮气排净装置中的空气,其目的是防止CO与空气混合加热爆炸
②该套装置中有不完善之处,还应在装置(Ⅳ)后补充尾气处理装置装置.
Ⅱ.该课外小组设计的从ZnSO4、FeCl3的混合溶液中制取ZnSO4•7H2O过程如下:
a.在混合液中加入6mol•L-1NaOH溶液,至pH=8为止.
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀.
c.向洗涤后的沉淀中加入2mol•L-1的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液.
d.滤液中加入2mol•L-1的硫酸,使其pH=2.
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列问题:
(1)步骤b中如何检验沉淀已经洗涤干净取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净
(2)步骤d中加入硫酸,使其pH=2的目的是抑制Zn2+的水解; 要制得ZnSO4•7H2O的步骤d还缺少的操作是将溶液加热浓缩,冷却结晶.

(1)写出用硝酸制取一氧化氮的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(2)查资料得知,HCOOH$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+H2O.实验室有如图1所示的装置,制取CO气体可选用的装置为A(填序号),实验室利用该装置还可制取的常见气体有Cl2(填写一种气体的分子式).
(3)查资料得知,利用催化剂可使汽车尾气中的一氧化碳和氮氧化物大部分发生反应转化为二氧化碳和氮气.该小组在实验室模拟汽车尾气处理,设计了如图2所示装置(部分夹持和装置已略去).
①实验前关闭旋塞K,先通氮气排净装置中的空气,其目的是防止CO与空气混合加热爆炸
②该套装置中有不完善之处,还应在装置(Ⅳ)后补充尾气处理装置装置.
Ⅱ.该课外小组设计的从ZnSO4、FeCl3的混合溶液中制取ZnSO4•7H2O过程如下:
a.在混合液中加入6mol•L-1NaOH溶液,至pH=8为止.
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀.
c.向洗涤后的沉淀中加入2mol•L-1的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液.
d.滤液中加入2mol•L-1的硫酸,使其pH=2.
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Fe (OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
(2)步骤d中加入硫酸,使其pH=2的目的是抑制Zn2+的水解; 要制得ZnSO4•7H2O的步骤d还缺少的操作是将溶液加热浓缩,冷却结晶.
8. 碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)═6AlCl(g)+6CO(g)△H=a kJ•mol-1
3AlCl(g)═2Al(l)+AlCl3(g)△H=b kJ•mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=0.5a+b kJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①0~10min内,NO的平均反应速率v(NO)=0.032mol•L-1•min-1,T1℃时,该反应的平衡常数K=0.25;
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是a d(填字母编号).
a.通入一定量的NO b.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q<0(填“>”或“<”).
④在恒容条件下,能判断该反应一定达到化学平衡状态的依据是b、c(填选项编号).
a.单位时间内生成2nmol NO(g)的同时消耗nmol CO2(g)
b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变
d.反应体系的压强不再发生改变
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示:请写出该电池正极反应式Ag2O+2e-+H2O=2Ag+2OH-;常温下,用该化学电源和惰性电极电解300ml硫酸铜溶液(过量),消耗27mg Al,则电解后溶液的pH=2(不考虑溶液体积的变化).
 碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)═6AlCl(g)+6CO(g)△H=a kJ•mol-1
3AlCl(g)═2Al(l)+AlCl3(g)△H=b kJ•mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=0.5a+b kJ•mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(min) 浓度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是a d(填字母编号).
a.通入一定量的NO b.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q<0(填“>”或“<”).
④在恒容条件下,能判断该反应一定达到化学平衡状态的依据是b、c(填选项编号).
a.单位时间内生成2nmol NO(g)的同时消耗nmol CO2(g)
b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变
d.反应体系的压强不再发生改变
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示:请写出该电池正极反应式Ag2O+2e-+H2O=2Ag+2OH-;常温下,用该化学电源和惰性电极电解300ml硫酸铜溶液(过量),消耗27mg Al,则电解后溶液的pH=2(不考虑溶液体积的变化).
7.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.00mol•L-1NaCl溶液中含有Na+的数目为NA | |
| B. | 常压下常温,6.4g由氧气和臭氧组成的混合物中含有的分子总数为0.2NA | |
| C. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| D. | 7.8g过氧化钠含有的共用电子对数为0.1NA |
6.化学与人类生产、生活,社会可持续发展密切相关.下列说法正确的是( )
| A. | 蔬菜表面洒少许福尔马林,可保鲜和消毒 | |
| B. | 绿色食品就是不使用化肥农药,不含任何化学物质的食品 | |
| C. | 光催化水制氢比电解水制氢更节能环保 | |
| D. | 光化学烟雾不会引起呼吸道疾病 |
5. 在容积恒定的密闭容器中进行反应 2NO+O2=2NO2 该反应的反应速率随时间变化的关系如图所示.若t2、t4时刻只改变一个条件,下列说法正确的是( )
在容积恒定的密闭容器中进行反应 2NO+O2=2NO2 该反应的反应速率随时间变化的关系如图所示.若t2、t4时刻只改变一个条件,下列说法正确的是( )
0 171736 171744 171750 171754 171760 171762 171766 171772 171774 171780 171786 171790 171792 171796 171802 171804 171810 171814 171816 171820 171822 171826 171828 171830 171831 171832 171834 171835 171836 171838 171840 171844 171846 171850 171852 171856 171862 171864 171870 171874 171876 171880 171886 171892 171894 171900 171904 171906 171912 171916 171922 171930 203614
 在容积恒定的密闭容器中进行反应 2NO+O2=2NO2 该反应的反应速率随时间变化的关系如图所示.若t2、t4时刻只改变一个条件,下列说法正确的是( )
在容积恒定的密闭容器中进行反应 2NO+O2=2NO2 该反应的反应速率随时间变化的关系如图所示.若t2、t4时刻只改变一个条件,下列说法正确的是( )| A. | 在t5时,容器NO2的体积分数是整个过程中的最大值 | |
| B. | 在t2时,采取的措施可以是增大压强 | |
| C. | 在t3~t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态 | |
| D. | 在t1~t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态 |

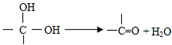 ,如图中X分子式为C4H2Br2O4,为六元环化合物,核磁共振氢谱表明其分子中只有一种类型H原子的吸收峰.
,如图中X分子式为C4H2Br2O4,为六元环化合物,核磁共振氢谱表明其分子中只有一种类型H原子的吸收峰.
 .它可以发生ab反应(填字母)a、取代 b、消去c、加成
.它可以发生ab反应(填字母)a、取代 b、消去c、加成 .
.