3.实验室中用苯甲醛制备苯甲醇和苯甲酸.
已知:①制备原理为:
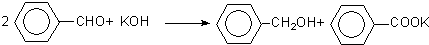
②有关物质的性质如表:
③醛可以与饱和NaHSO3溶液反应生成难溶于有机物而易溶于水的钠盐.
④纯净的液态有机物一般都有固定沸点.
制备苯甲醇和苯甲酸的主要过程如图:

(1)操作I的名称是分液.操作II的名称是蒸馏.
(2)操作III的名称是过滤,产品乙是苯甲酸.
(3)某同学测定产品甲的沸点,发现其在190℃即开始沸腾.该同学推测产品甲是苯甲醇与苯甲醛的混合物,设计了如下方案进行检验和提纯,结果表明推测正确.请在答题卡上完成表中内容.
(4)纯度测定:称取7.00g产品甲,加入足量银氨溶液充分反应,生成单质Ag 2.16g.则产品甲中苯甲醇的质量分数的计算表达式为:$\frac{7.00g-\frac{2.16g}{108g/mol}×\frac{1}{2}×106g/mol}{7.00g}$100%,
计算结果为84.9%(保留三个有效数字.苯甲醛相对分子质量:106;Ag:108).
已知:①制备原理为:

②有关物质的性质如表:
| 物质 | 沸点 | 熔点 | 溶解性 |
| 苯甲醛 | 179℃ | -26℃ | 微溶于水,能与乙醚混溶. |
| 苯甲醇 | 205.3℃ | -15.3℃ | 稍溶于水,能与乙醚混溶 |
| 苯甲酸 | 249℃ | 122℃ | 微溶于水,易溶于乙醚. |
| 乙醚 | 34.8℃ | 难溶于水 |
④纯净的液态有机物一般都有固定沸点.
制备苯甲醇和苯甲酸的主要过程如图:

(1)操作I的名称是分液.操作II的名称是蒸馏.
(2)操作III的名称是过滤,产品乙是苯甲酸.
(3)某同学测定产品甲的沸点,发现其在190℃即开始沸腾.该同学推测产品甲是苯甲醇与苯甲醛的混合物,设计了如下方案进行检验和提纯,结果表明推测正确.请在答题卡上完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| 步骤① | 取少量产品甲于洁净的试管中,再加入2mLAg(NH3)OH 溶液,水浴加热. | 试管内壁产生光亮银镜 | 产品甲中含有苯甲醛 |
| 步骤② | 将少量产品甲置于分液漏斗中,然后向漏斗中加入饱和NaHSO3溶液,溶液,充分反应后分液. | ||
| 步骤③ | 将步骤②的有机层洗涤、干燥后,测定产品的 沸点 | 沸点为205.3℃ | 所得有机层是纯净的苯甲醇 |
计算结果为84.9%(保留三个有效数字.苯甲醛相对分子质量:106;Ag:108).
13.石蕊(用HIn表示)是一种常用的酸性指示剂,其电离方程式为HIn?H++In-,已知它在pH<5的溶液中呈红色,在pH>8的溶液中呈蓝色,下列判断中不正确的是( )
| A. | HIn呈红色 | B. | In-呈蓝色 | ||
| C. | 加入碱溶液后n(In-)增大 | D. | HIn呈蓝色 |
12.温度为T℃,压强为1.01×106Pa条件下,某密闭容器下列反应达到化学平衡A(g)+aB(?)?4C(g),达到化学平衡时测得c(A)=0.2mol•L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.36mol•L-1;若继续压缩容器,使压强增大到5.05×106Pa,第三次达到平衡时,测得c(A)=1.1mol•L-1;则下列关于有关说法不正确的是( )
0 171551 171559 171565 171569 171575 171577 171581 171587 171589 171595 171601 171605 171607 171611 171617 171619 171625 171629 171631 171635 171637 171641 171643 171645 171646 171647 171649 171650 171651 171653 171655 171659 171661 171665 171667 171671 171677 171679 171685 171689 171691 171695 171701 171707 171709 171715 171719 171721 171727 171731 171737 171745 203614
| A. | 第二次平衡时B为气态 | |
| B. | a>3 | |
| C. | 第一次平衡后增大压强平衡向左移动 | |
| D. | 第三次达到平衡时B可能为非气态 |
 实验室制溴化亚铁可以用图示的装置:装置中A为CO2发生装置;D和d中均盛有液溴;E为外套电炉丝的不锈钢管;e是两只耐高温的瓷皿,其中共盛有56g细铁粉.实验开始时先将铁粉加热至600~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,随反应的进行将d中液溴滴入到D中.经过几个小时的连续反应,在钢管的一端沉积有80g黄绿色鳞片状溴化亚铁.(溴的沸点:58.78℃,并对有机物有腐蚀性)
实验室制溴化亚铁可以用图示的装置:装置中A为CO2发生装置;D和d中均盛有液溴;E为外套电炉丝的不锈钢管;e是两只耐高温的瓷皿,其中共盛有56g细铁粉.实验开始时先将铁粉加热至600~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,随反应的进行将d中液溴滴入到D中.经过几个小时的连续反应,在钢管的一端沉积有80g黄绿色鳞片状溴化亚铁.(溴的沸点:58.78℃,并对有机物有腐蚀性)