16. 硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:
硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:
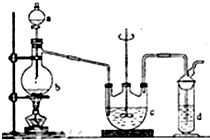
2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,实验室模拟该工业过程的装置如图所示,回答下列问题:
(1)b中反应的离子方程式为SO32-+2H+=H2O+SO2↑或HSO3-+H+=SO2↑+H2O,c中试剂为硫化钠和碳酸钠的混合溶液.
(2)反应开始后,c中先有浑浊产生,后又变为澄清,此浑浊物是S.
(3)控制b中的溶液的pH接近7,停止通入SO2.若未控制好pH<7,会影响产率,原因是(用离子方程式表示)S2O32-+2H+=S↓+H2O+SO2↑
(4)停止通入SO2后,将c中的溶液抽入d中,d中的试剂为NaOH溶液.
(5)将d所得液溶转移到蒸发皿中,水浴加热浓缩,冷却结晶、过滤、洗涤,洗涤晶体所用的试剂为(填化学式)C2H5OH.
(6)实验中要控制SO2生成速率,可采取的措施有控制反应温度、调节酸的滴加速度或调节酸的浓度等;(写出一条)
(7)为检验制得的产品的纯度,该实验小组称取5.0克的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL0.01mol/LKIO3溶液,并加入过量的KI酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时达到滴定终点.实验数据如下表:
则该产品的纯度是59.3%,(用百分数表示,保留1位小数)间接碘量法滴定过程中可能造成实验结果偏低的是AB
A.滴定管未用Na2S2O3溶液润洗
B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗
D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡.
 硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:
硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,实验室模拟该工业过程的装置如图所示,回答下列问题:
(1)b中反应的离子方程式为SO32-+2H+=H2O+SO2↑或HSO3-+H+=SO2↑+H2O,c中试剂为硫化钠和碳酸钠的混合溶液.
(2)反应开始后,c中先有浑浊产生,后又变为澄清,此浑浊物是S.
(3)控制b中的溶液的pH接近7,停止通入SO2.若未控制好pH<7,会影响产率,原因是(用离子方程式表示)S2O32-+2H+=S↓+H2O+SO2↑
(4)停止通入SO2后,将c中的溶液抽入d中,d中的试剂为NaOH溶液.
(5)将d所得液溶转移到蒸发皿中,水浴加热浓缩,冷却结晶、过滤、洗涤,洗涤晶体所用的试剂为(填化学式)C2H5OH.
(6)实验中要控制SO2生成速率,可采取的措施有控制反应温度、调节酸的滴加速度或调节酸的浓度等;(写出一条)
(7)为检验制得的产品的纯度,该实验小组称取5.0克的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL0.01mol/LKIO3溶液,并加入过量的KI酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时达到滴定终点.实验数据如下表:
| 实验序号 | 1 | 2 | 3 |
| Na2S2O3溶液体积(mL) | 19.98 | 20.02 | 21.18 |
A.滴定管未用Na2S2O3溶液润洗
B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗
D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡.
14.钛铁矿的主要成分为FeTiO3(可表示为FeO•TiO2),含有少量MgO、SiO2等杂质.利用钛铁矿制备二氧化钛,进一步制备钛单质,流程如图:

已知:FeTiO3+4H+=Fe2++TiO2++2H2O草酸(C2H2O4)具有很强还原性,易被氧化成二氧化碳
(1)化合物FeTiO3中铁元素的化合价是+2.
(2)钛铁矿加入过量H2SO4后,得到的滤渣A为SiO2(填化学式).
(3)含TiO2+溶液乙转化生成TiO2的离子方程式是TiO2-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2↓+2H+.
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是20:9.
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数为$\frac{cV×10{\;}^{-3}×M}{w}$×100%(用代数式表示).
(6)TiO2制取单质Ti,涉及到的步骤如下:TiO2$\stackrel{①}{→}$TiCl4$→_{Mg_{800}℃}^{②}$Ti
反应②的方程式是TiCl4+2Mg$\frac{\underline{\;800℃\;}}{\;}$2MgCl2+Ti,由TiCl4→Ti需要在Ar气中进行的理由是高温下Mg(Ti)会与空气中的O2(或CO2、N2)作用.反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据表中信息,需加热的温度略高于1412℃即可.

已知:FeTiO3+4H+=Fe2++TiO2++2H2O草酸(C2H2O4)具有很强还原性,易被氧化成二氧化碳
(1)化合物FeTiO3中铁元素的化合价是+2.
(2)钛铁矿加入过量H2SO4后,得到的滤渣A为SiO2(填化学式).
(3)含TiO2+溶液乙转化生成TiO2的离子方程式是TiO2-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2↓+2H+.
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是20:9.
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/L NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数为$\frac{cV×10{\;}^{-3}×M}{w}$×100%(用代数式表示).
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
反应②的方程式是TiCl4+2Mg$\frac{\underline{\;800℃\;}}{\;}$2MgCl2+Ti,由TiCl4→Ti需要在Ar气中进行的理由是高温下Mg(Ti)会与空气中的O2(或CO2、N2)作用.反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据表中信息,需加热的温度略高于1412℃即可.
12. Na2S2O4是重要的工业漂白剂,某化学小组欲制备Na2S2O4(如图)并探究其性质.现将1.5mol/L的HCOONa溶液和0.5mol/L NaOH溶液等体积注入三颈烧瓶,发生反应:HCOONa+2SO2+NaOH═Na2S2O4+CO2+H2O
Na2S2O4是重要的工业漂白剂,某化学小组欲制备Na2S2O4(如图)并探究其性质.现将1.5mol/L的HCOONa溶液和0.5mol/L NaOH溶液等体积注入三颈烧瓶,发生反应:HCOONa+2SO2+NaOH═Na2S2O4+CO2+H2O
(l)a装置的名称:分液漏斗;c装置的目的吸收二氧化硫,防止污染空气.
(2)b中制SO2的化学方程式为-_Na2SO3+H2SO4(浓)═Na2SO4+H2O+SO2↑_;控制b中反应速率的方法是通过分液漏斗颈部活塞控制低价硫酸的快慢.
(3)当三颈烧瓶中溶液接近中性时停止通人气体,蒸发得到固体产品.取1.0g固体产品溶于5mL水中,加入1mL的银氨溶液,振荡,水浴10s出现银镶.
甲同学得出结论:10s时Na2S2O4银氨溶液反应形成银镜.
乙同学认为上述实验不能说甲的结论一定成立,其依据可能是因为HCOONa过量,分离出的晶体所含杂质HCOONa具有还原性也能发生银镜反应.
针对甲、乙同学的分歧,丙同学取该实验所得固体设计如下实验方案,请你帮助完成:
0 171047 171055 171061 171065 171071 171073 171077 171083 171085 171091 171097 171101 171103 171107 171113 171115 171121 171125 171127 171131 171133 171137 171139 171141 171142 171143 171145 171146 171147 171149 171151 171155 171157 171161 171163 171167 171173 171175 171181 171185 171187 171191 171197 171203 171205 171211 171215 171217 171223 171227 171233 171241 203614
 Na2S2O4是重要的工业漂白剂,某化学小组欲制备Na2S2O4(如图)并探究其性质.现将1.5mol/L的HCOONa溶液和0.5mol/L NaOH溶液等体积注入三颈烧瓶,发生反应:HCOONa+2SO2+NaOH═Na2S2O4+CO2+H2O
Na2S2O4是重要的工业漂白剂,某化学小组欲制备Na2S2O4(如图)并探究其性质.现将1.5mol/L的HCOONa溶液和0.5mol/L NaOH溶液等体积注入三颈烧瓶,发生反应:HCOONa+2SO2+NaOH═Na2S2O4+CO2+H2O(l)a装置的名称:分液漏斗;c装置的目的吸收二氧化硫,防止污染空气.
(2)b中制SO2的化学方程式为-_Na2SO3+H2SO4(浓)═Na2SO4+H2O+SO2↑_;控制b中反应速率的方法是通过分液漏斗颈部活塞控制低价硫酸的快慢.
(3)当三颈烧瓶中溶液接近中性时停止通人气体,蒸发得到固体产品.取1.0g固体产品溶于5mL水中,加入1mL的银氨溶液,振荡,水浴10s出现银镶.
甲同学得出结论:10s时Na2S2O4银氨溶液反应形成银镜.
乙同学认为上述实验不能说甲的结论一定成立,其依据可能是因为HCOONa过量,分离出的晶体所含杂质HCOONa具有还原性也能发生银镜反应.
针对甲、乙同学的分歧,丙同学取该实验所得固体设计如下实验方案,请你帮助完成:
| 实验步骤 | 现象及结论 |
| 步骤Ⅰ:对三颈烧瓶分离出的产品进行重结晶得到纯净的Na2S2O4(仅需说明方法) | |
| 步骤Ⅱ:取0.1g步骤Ⅰ的产品溶于5mL银氨溶液,振荡,水浴加热10s,观察现象 | 若10S出现银镜,则甲的结论正确(或Na2S2O4具有还原性),反之则乙正确 |


 氯化亚锡有广泛的用途,工业可用作催化剂、脱氧剂等.如下是某实验室常用的一种制取无水氯化亚锡的步骤:
氯化亚锡有广泛的用途,工业可用作催化剂、脱氧剂等.如下是某实验室常用的一种制取无水氯化亚锡的步骤:



 某小组以工业氧化铁、草酸、盐酸、异丙醚为原料,合成晶体X[化学式为Fe2(C2O4)3•5H2O],并确定其纯度.
某小组以工业氧化铁、草酸、盐酸、异丙醚为原料,合成晶体X[化学式为Fe2(C2O4)3•5H2O],并确定其纯度.