14.已知丙烷的二氯代物C3H6Cl2有4种同分异构体,则分子式为C3H2Cl6的同分异构体共有(不考虑立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
13.下列实验操作错误的是( )
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 滴定时,左手控制滴定管活塞,右手握持锥形瓶,眼睛注视滴定管中的液面 | |
| D. | 用精密pH试纸测得溶液的pH为4.2 |
10.有A、B两种原子,B原子的M层比A原子的M层多3个电子,B原子L层电子数恰为A原子L层电子数的2倍.A和B分别是( )
| A. | 硅原子和钠原子 | B. | 硼原子和氦原子 | C. | 氯原子和碳原子 | D. | 碳原子和铝原子 |
9.下列说法正确的是( )
| A. | 反应焓变是指1 g物质参加反应时的能量变化 | |
| B. | 当反应放热时,△H>0,反应吸热时,△H<0 | |
| C. | 在加热条件下发生的反应均为吸热反应 | |
| D. | 一个化学反应中,当反应物总能量大于反应产物总能量时,反应放热,△H为“-” |
7.工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g)
(1)已知在25.C时:
C(石墨,s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-111kJ•mol-1
C(石墨,s)+O2(g)═CO2(g)△H2=-494kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H3=-142kJ•mol-1
则反应CO(g)+H2O(g)═CO2(g)+H2(g)的反应热△H=-241kJ•mol-1(3分)
(2)现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
①以下反应能说明CO(g)+H2O(g)?CO2(g)+H2(g)达到平衡状态的是a
A.容器中CO的含量保持不变 B.容器中CO2浓度与CO浓度相等
C.ν(CO)正=ν(H2O )正 D.容器中混合气体的平均相对分子质量保持不变
②实验Ⅰ中,从反应开始到反应达到平衡时,CO的平均反应速率ν(CO)=0.16mol/(L.min);;
③实验Ⅱ条件下反应的平衡常数K=0.33(保留小数点后二位).若降低温度,化学平衡常数K将增大(填“增大”“减小”或“不变”).
④实验Ⅲ中,若平衡时,CO的转化率大于水蒸气,则a,b必须满足的关系是a<b;
⑤若在900℃时,实验Ⅱ反应达到平衡后,向此容器中再加入1molCO、0.5mol H2O、0.2mol CO2、0.5mol H2,则此时ν(正)>ν(逆)(填“>”或“<”),平衡向正反应方向移动(填“正反应”“逆反应”“不移动”)
(1)已知在25.C时:
C(石墨,s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-111kJ•mol-1
C(石墨,s)+O2(g)═CO2(g)△H2=-494kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H3=-142kJ•mol-1
则反应CO(g)+H2O(g)═CO2(g)+H2(g)的反应热△H=-241kJ•mol-1(3分)
(2)现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
| 实验组 | 温度℃ | 超始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
| 2 | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
| 3 | 900 | a | b | c | d | t |
A.容器中CO的含量保持不变 B.容器中CO2浓度与CO浓度相等
C.ν(CO)正=ν(H2O )正 D.容器中混合气体的平均相对分子质量保持不变
②实验Ⅰ中,从反应开始到反应达到平衡时,CO的平均反应速率ν(CO)=0.16mol/(L.min);;
③实验Ⅱ条件下反应的平衡常数K=0.33(保留小数点后二位).若降低温度,化学平衡常数K将增大(填“增大”“减小”或“不变”).
④实验Ⅲ中,若平衡时,CO的转化率大于水蒸气,则a,b必须满足的关系是a<b;
⑤若在900℃时,实验Ⅱ反应达到平衡后,向此容器中再加入1molCO、0.5mol H2O、0.2mol CO2、0.5mol H2,则此时ν(正)>ν(逆)(填“>”或“<”),平衡向正反应方向移动(填“正反应”“逆反应”“不移动”)
6.2010年10月1日,我国在西昌卫星发射中心成功发射“嫦娥二号”.嫦娥二号火箭推进器以联氨(N2H4)为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式为
N2H4(g)+O2(g)═N2(g)+2H2O(g);△H1=-533.23kJ•mol-1
H2O(g)═H2O(l);△H2=-44kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g);△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
0 171002 171010 171016 171020 171026 171028 171032 171038 171040 171046 171052 171056 171058 171062 171068 171070 171076 171080 171082 171086 171088 171092 171094 171096 171097 171098 171100 171101 171102 171104 171106 171110 171112 171116 171118 171122 171128 171130 171136 171140 171142 171146 171152 171158 171160 171166 171170 171172 171178 171182 171188 171196 203614
N2H4(g)+O2(g)═N2(g)+2H2O(g);△H1=-533.23kJ•mol-1
H2O(g)═H2O(l);△H2=-44kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g);△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
| A. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l);△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g);△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l);△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g);△H=-817.63 kJ•mol-1 |
 100mL某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,会产生H2;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则(1)溶液中一定含有的阳离子有H+、NH4+、Mg2+、Al3+,一定不含有的离子有CO32-、NO3-、Fe3+.
100mL某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,会产生H2;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则(1)溶液中一定含有的阳离子有H+、NH4+、Mg2+、Al3+,一定不含有的离子有CO32-、NO3-、Fe3+. E的氢化物的电子式
E的氢化物的电子式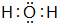 .
.