13.乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平.结合如图1路线回答:
已知:2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH
(1)反应II的化学方程式是2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(2)D为高分子化合物,可以用来制造多种包装材料,其结构简式是 .
.
(3)E是有香味的物质,在实验室用图2装置制取.
①反应IV的化学方程式是CH3COOH+HOCH2CH3 CH3COOCH2CH3+H2O,该反应类型为酯化反应或取代反应.
CH3COOCH2CH3+H2O,该反应类型为酯化反应或取代反应.
②该装置图中有一个明显的错误是导气管的出口伸入到饱和碳酸钠溶液液面以下.
(4)为了证明浓硫酸在反应IV中起到了催化剂和吸水剂的作用,某同学利用上图改进后装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.实验D中应加入盐酸的体积和浓度分别是3mL和4 mol•L-1.
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.

已知:2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH
(1)反应II的化学方程式是2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(2)D为高分子化合物,可以用来制造多种包装材料,其结构简式是
 .
.(3)E是有香味的物质,在实验室用图2装置制取.
①反应IV的化学方程式是CH3COOH+HOCH2CH3
 CH3COOCH2CH3+H2O,该反应类型为酯化反应或取代反应.
CH3COOCH2CH3+H2O,该反应类型为酯化反应或取代反应.②该装置图中有一个明显的错误是导气管的出口伸入到饱和碳酸钠溶液液面以下.
(4)为了证明浓硫酸在反应IV中起到了催化剂和吸水剂的作用,某同学利用上图改进后装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
| 实验编号 | 试管甲中试剂 | 试管乙中试剂 | 有机层的厚度/cm |
| A | 2mL乙醇、1mL乙酸、 1mL18mol•L-1 浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、 3mL 2mol•L-1 H2SO4 | 0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.

12.做电解水实验时,为了增强水的导电能力,可以加入的试剂是( )
| A. | CuSO4 | B. | KCl | C. | KOH | D. | K2SO4 |
10.下列各组物质性质的比较中,正确的是( )
| A. | 热稳定性:NH3<PH3<H2O | |
| B. | P元素最高价氧化物对应的水化物酸性比Cl的强 | |
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | |
| D. | 元素非金属性:O>F |
9.下列说法正确的是( )
| A. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 | |
| B. | 可逆反应达到平衡后,正、逆反应速率均为0 | |
| C. | 2 mol SO2 与1 mol O2混合一定能生成2 mol SO3 | |
| D. | 使用催化剂不一定能加大反应速率 |
8.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
0 170761 170769 170775 170779 170785 170787 170791 170797 170799 170805 170811 170815 170817 170821 170827 170829 170835 170839 170841 170845 170847 170851 170853 170855 170856 170857 170859 170860 170861 170863 170865 170869 170871 170875 170877 170881 170887 170889 170895 170899 170901 170905 170911 170917 170919 170925 170929 170931 170937 170941 170947 170955 203614
| A. | 100 mL 0.1 mol•L-1 Na2SO4溶液中,粒子总数是0.03NA | |
| B. | 常温常压下,32 g O2-中所含电子的数目为17NA | |
| C. | 1 mol Al3+完全水解生成氢氧化铝胶体粒子的数目为NA | |
| D. | 标准状况下,分子数为NA的N2、C2H4混合气体的质量无法确定 |

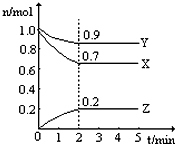 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
 用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g•mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g•mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.