2.将0.5mol•L-1的Na2CO3溶液与amol•L-1的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断正确的是( )
| A. | c(Na+)>2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | 若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则可确定a>0.5 | |
| D. | 若c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c (H2CO3),则可确定a=0.5 |
1.为了除去FeSO4溶液中的Fe3+,可用加入纯铁屑,但此法很费时;现有一种方法是在蒸馏水沸腾时加入粉未状的绿矾(少量多次),搅拌,直到观察到有褐色沉淀产生即可停止加入药品,煮沸1~2分钟,趁热过滤,密封保存所得的FeSO4溶液,此法的原理是( )
| A. | Fe3+易水解,它的水解产物之一能抑制的Fe2+水解 | |
| B. | Fe2+有较强的还原性,它能还原Fe3+ | |
| C. | Fe3+有较强的氧化性,它能氧化Fe2+ | |
| D. | Fe3+的水解是吸热反应,升温能促进它的水解 |
20.下列实验现象描述正确的是( )
| A. | 电解氯化铜溶液,将阳极气体产物通入碘化钾淀粉溶液中,溶液变蓝 | |
| B. | 红热的铜丝在氯气中燃烧,产生了棕黄色的雾 | |
| C. | 碘水中加入少量裂化汽油振荡,静置后上层颜色变浅,下层颜色变为紫红色 | |
| D. | 向含有苯酚的苯溶液中滴入少量浓溴水,产生了白色沉淀 |
19.下列离子方程式中正确的是( )
| A. | 向硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-→CuS↓+H2S↑ | |
| B. | Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+→Fe2++2Fe3++4H2O | |
| C. | 碳酸氢铵溶液与苛性钾溶液混和共热:NH4++OH-→NH3↑+H2O | |
| D. | 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O→SO32-+2HClO |
18.工业上制备下列金属,采用的化学反应原理正确的是( )
| A. | 镁:2MgO (熔融)$\stackrel{通直流电}{→}$Mg+O2↑ | B. | 钙:CaO+C$\stackrel{高温}{→}$Ca+CO↑ | ||
| C. | 锰:3MnO2+4Al$\stackrel{高温}{→}$3Mn+2Al2O3 | D. | 汞:HgS$\stackrel{加热}{→}$Hg+S |
17.氮化钠(Na3N)晶体熔融时能导电.下列描述正确的是( )
| A. | 构成晶体的两种微粒电子层结构相同 | |
| B. | 构成晶体的两种微粒半径相等 | |
| C. | 构成晶体的两种微粒的核外电子能量相同 | |
| D. | 构成晶体的两种微粒的电子层数不同 |
16.捕碳技术是指从空气中捕获CO2的技术.目前NH3已经被用作工业捕碳剂.下列物质中不能作为捕碳剂的是( )
0 170271 170279 170285 170289 170295 170297 170301 170307 170309 170315 170321 170325 170327 170331 170337 170339 170345 170349 170351 170355 170357 170361 170363 170365 170366 170367 170369 170370 170371 170373 170375 170379 170381 170385 170387 170391 170397 170399 170405 170409 170411 170415 170421 170427 170429 170435 170439 170441 170447 170451 170457 170465 203614
| A. | 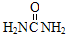 | B. | H2NCH2CH2NH2 | C. | (NH4)2CO3 | D. | Na2CO3 |
 (不考虑立体结构).M的新旧二条合成路线如下:
(不考虑立体结构).M的新旧二条合成路线如下:



 D
D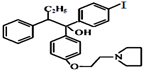
 有多种同分异构体,其中满足①遇FeCl3显色②苯环上的一溴取代物只有一种,符合条件的同分异构体数目有多少种.6任写其中一种的结构简式.
有多种同分异构体,其中满足①遇FeCl3显色②苯环上的一溴取代物只有一种,符合条件的同分异构体数目有多少种.6任写其中一种的结构简式. 中任一种
中任一种 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +HBr
+HBr 及含二个碳原子的有机化合物为原料,制备芳香醇
及含二个碳原子的有机化合物为原料,制备芳香醇 的合成路线(不超过5步反应).
的合成路线(不超过5步反应).
 DCH3COOOH
DCH3COOOH .
. 烟气的脱硫(除SO2)和脱硝(除NOx)都是环境科学研究的热点.可以通过氧化还原反应或酸碱反应进行脱硫和脱硝.
烟气的脱硫(除SO2)和脱硝(除NOx)都是环境科学研究的热点.可以通过氧化还原反应或酸碱反应进行脱硫和脱硝.