5.将0.1mol•L-1的氨水加水稀释至0.01mol•L-1,稀释过程中温度不变,下列叙述正确的是( )
| A. | 稀释后溶液中的c(H+)和c(OH-)均减小 | |
| B. | 稀释过程中氨水的电离平衡向左移动 | |
| C. | 稀释后溶液中c(OH-)变为稀释前的$\frac{1}{10}$ | |
| D. | 稀释过程中溶液中$\frac{[0{H}^{-}]}{[N{H}_{3}•{H}_{2}O]}$增大 |
3.下列化学用语中,书写或说法正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 丙烷的球棍模型为 | |
| C. | 乙醇含有的官能团是-OH,带一个单位负电荷 | |
| D. | 乙酸的分子式为C2H4O2,其中CH3-在溶液中能电离出H+ |
1.一定温度下,将3mol PCl3和 1.5mol Cl2充入容积不变的密闭容器中,在一定条件下反应:PCl3+Cl2?PCl5.各物质均为气态.达平衡后,PCl5为0.4mol.若此时再移走1.5mol PCl3 和0.75mol Cl2,相同温度下达到平衡,PCl5的物质的量为( )
| A. | 0.4mol | B. | 0.2mol | C. | 0.2mol<x<0.4mol | D. | <0.2mol |
13.下列排列顺序正确的是( )
| A. | 常温下将0.1mol•L-1NH4Cl溶液与0.05mol•L-1NaOH溶液等体积混合:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 常温下物质的量浓度相等的①NH4HSO4②CH3COONH4③NH4Cl三种溶液中c(NH4+):①>③>② | |
| C. | 0.1mol•L-1的NaHA溶液,其pH=11,则溶液中:c(HA-)>c(OH-)>c(A2-)>c(H2A) | |
| D. | 在相同条件下,将足联AgCl加入等体积的①0.01mol•L-1 KCl②0.1mol•L-1 KCl溶液③蒸馏水三种液体中,所能溶解的AgCl质量关系为:①>②>③ |
12.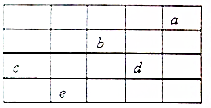 如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )
如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )
 如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )
如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )| A. | b元素除0价外,只有一种化合价 | |
| B. | 五种元素中,c元素的天然氧化物可被称为刚玉 | |
| C. | b、d气态氢化物溶于水,溶液的酸性:b>d | |
| D. | c、d气态氢化物的稳定性:d>c |
11.下列对第115号元素的分析和推断中正确的是( )
| A. | 该元素位于第七周期ⅥA族 | |
| B. | 该元素较易与氢结合为气态氢化物 | |
| C. | 该元素属于金属元素 | |
| D. | 该元素(R)最高价氧化物对应的水化物化学式为H2RO3 |
10.黄铁矿的主要成分是FeS2,FeS2读作“过硫化亚铁”,它是离子化合物,其中有类似于Na2O2结构,则下列说法中正确的是( )
0 170263 170271 170277 170281 170287 170289 170293 170299 170301 170307 170313 170317 170319 170323 170329 170331 170337 170341 170343 170347 170349 170353 170355 170357 170358 170359 170361 170362 170363 170365 170367 170371 170373 170377 170379 170383 170389 170391 170397 170401 170403 170407 170413 170419 170421 170427 170431 170433 170439 170443 170449 170457 203614
| A. | 与盐酸反应的化学方程式为:FeS2+2HCl═FeCl2+S↓+H2S↑ | |
| B. | 在FeS2中,硫元素的化合价与辉铜矿(主要成分是Cu2S)中硫元素的化合价相同 | |
| C. | FeS2中的Fe元素位于第4周期第ⅧB族 | |
| D. | 若FeS2在空气中燃烧时生成Fe2O3和SO2,则1mol FeS2在反应中将失去6mol e- |

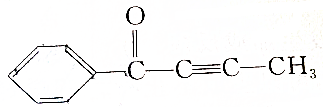 ,请回答下列问题:
,请回答下列问题: