6.设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有( )
| A. | 12g金刚石中含4NA个C-C共价键 | |
| B. | 2L 0.5 moI.L-1盐酸溶液所含的HCI分子数目为NA | |
| C. | 标准状况下,2.24LCL4含有的原子数为0.5NA | |
| D. | 7.1 gCL2与5.6 g Fe反应,转移的电子总数为0,2NA |
5.下列离子方程式中,正确的是( )
| A. | 大理石溶解于醋酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 澄清石灰水中加入CuSO4溶液混合 2OH-+Cu2+═Cu(OH)2↓ | |
| C. | NaHSO4溶液和Na2CO3溶液混合 2H++CO32-═CO2↑+H2O | |
| D. | NaHSO4溶液中加入Ba(OH)2═Ba2++SO42-═BaSO4↓ |
4.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1molCl2与足量Fe反应转移电子数一定为3NA | |
| B. | 标准状况下,22.4L NH3中含有共价键的数目为NA | |
| C. | 1.0L 1.0mol•L-1的Na2SiO3水溶液中含有的氧原子数为3NA | |
| D. | 4.6g Na完全转化成NaO和Na2O2的混合物,混合物中阴离子总数为0.1NA |
3.下列有关化学用语正确的是( )
| A. | O原子的电子排布图为 | |
| B. | 氯化钠的分子式:NaCl | |
| C. | Cl-的结构示意图: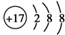 | |
| D. | Ca原子的电子排布式为 1s22s22p63s23p63d2 |
2.已知短周期元素(1~18号元素)的离子aA2+、bB+、cC3-、dD-具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径:A>B>C>D | B. | 原子序数:d>c>b>a | ||
| C. | 单质的还原性:A>B>D>C | D. | 离子半径:C>D>B>A |
1.在一定温度下,向饱和苛性钠溶液中加入一定量的过氧化钠,充分反应后恢复到原温度,下列有关说法中,正确的是( )
| A. | 溶液中Na+浓度增大,有O2放出 | B. | 溶液的碱性不变,有H2放出 | ||
| C. | 溶液中Na+数目减少,有O2放出 | D. | 溶液的碱性不变,有O2放出 |
20.下列分子中,所有原子都满足最外层8电子稳定结构的是( )
| A. | 光气(COCl2) | B. | 六氟化硫(SF6) | C. | 三氟化硼(BF3) | D. | 五氯化磷(PCl5) |
19.(一)对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系.下表为几种弱酸在25℃时的电离平衡常数
回答下列问题:
(1)K只与温度有关,当温度升高时,K值增大(填“增大”、“减小”、“不变”).
(2)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是H2PO4-,最弱的是HPO42-.
(3)对于同一种多元弱酸,有不止一个电离平衡常数,多个常数K1、K2、K3、之间存在某种大小关系,此关系是K1>K2>K3;以碳酸为例,用离子方程式和必要的文字说明产生此规律的原因多元弱酸分步电离,上一级电离产生的H+抑制下一级的电离,所以碳酸的二级电离常数小于一级电离常数:H2CO3?H++HCO3-,HCO3-?H++CO32-.
(4)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L CH3COOH的电离转化率为α,则该温度下醋酸的电离平衡常数K=${\;}_{C{H}_{3}COOH}$$\frac{c{α}^{2}}{1-α}$.
(二)化合物SOCl2是一种液态化合物,沸点77℃.在盛有10mL水的锥形瓶中,小心地滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出.该气体可使滴有品红试液的滤纸褪色.
(1)写出SOCl2和水反应的化学方程式:SOCl2+H2O=SO2↑+2HCl.
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是Al2O3;用SOCl2与AlCl3•6H2O混合共热得到无水AlCl3,原因是因为当与SOCl2混合共热时,由于SOCl2极易吸水,防止AlCl3的水解,同时产生的HCl也可以抑制AlCl3的水解.
0 169622 169630 169636 169640 169646 169648 169652 169658 169660 169666 169672 169676 169678 169682 169688 169690 169696 169700 169702 169706 169708 169712 169714 169716 169717 169718 169720 169721 169722 169724 169726 169730 169732 169736 169738 169742 169748 169750 169756 169760 169762 169766 169772 169778 169780 169786 169790 169792 169798 169802 169808 169816 203614
| 酸 | 电离平衡常数K |
| CH3COOH | 1.76×10-5 |
| H2CO3 | K1=4.31×10-7 K2=5.61×10-11 |
| H3PO4 | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
(1)K只与温度有关,当温度升高时,K值增大(填“增大”、“减小”、“不变”).
(2)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是H2PO4-,最弱的是HPO42-.
(3)对于同一种多元弱酸,有不止一个电离平衡常数,多个常数K1、K2、K3、之间存在某种大小关系,此关系是K1>K2>K3;以碳酸为例,用离子方程式和必要的文字说明产生此规律的原因多元弱酸分步电离,上一级电离产生的H+抑制下一级的电离,所以碳酸的二级电离常数小于一级电离常数:H2CO3?H++HCO3-,HCO3-?H++CO32-.
(4)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L CH3COOH的电离转化率为α,则该温度下醋酸的电离平衡常数K=${\;}_{C{H}_{3}COOH}$$\frac{c{α}^{2}}{1-α}$.
(二)化合物SOCl2是一种液态化合物,沸点77℃.在盛有10mL水的锥形瓶中,小心地滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出.该气体可使滴有品红试液的滤纸褪色.
(1)写出SOCl2和水反应的化学方程式:SOCl2+H2O=SO2↑+2HCl.
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是Al2O3;用SOCl2与AlCl3•6H2O混合共热得到无水AlCl3,原因是因为当与SOCl2混合共热时,由于SOCl2极易吸水,防止AlCl3的水解,同时产生的HCl也可以抑制AlCl3的水解.