题目内容
1.在一定温度下,向饱和苛性钠溶液中加入一定量的过氧化钠,充分反应后恢复到原温度,下列有关说法中,正确的是( )| A. | 溶液中Na+浓度增大,有O2放出 | B. | 溶液的碱性不变,有H2放出 | ||
| C. | 溶液中Na+数目减少,有O2放出 | D. | 溶液的碱性不变,有O2放出 |
分析 过氧化钠能与水反应,则饱和的烧碱溶液中的溶剂减少,原饱和溶液有晶体析出,剩余溶液还是饱和溶液,温度不变时,溶液中离子的浓度不变,但数目减少.
解答 解:因过氧化钠与水反应生成氢氧化钠和氧气,因为已经饱和,所以不会再溶解,浓度不变,但由于水的减少,水中Na+、OH-的数目减少.
A、原饱和溶液有晶体析出,剩余溶液还是饱和溶液,温度不变时,溶液中离子的浓度不变,即溶液中Na+浓度不变,有O2放出,故A错误;
B、原饱和溶液有晶体析出,剩余溶液还是饱和溶液,温度不变时,溶液中离子的浓度不变,即溶液中OH-浓度不变,碱性不变,有O2放出,故B错误;
C、溶液中Na+数目减小,有O2放出,故C正确;
D、溶液中OH-浓度不变,碱性不变,有O2放出,故D正确;
故选CD.
点评 本题考查过氧化钠与水的反应及饱和溶液的变化,明确饱和溶液中溶剂减少对溶液的影响是解答本题的关键,应抓住温度不变,饱和溶液析出晶体后剩余溶液仍然为饱和溶液来解答.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
11.下列关于化学键和分子间作用力的说法中不正确的是( )
| A. | 化学键是一种作用力 | |
| B. | 化学键可以使离子相结合,也可以使原子相结合 | |
| C. | 一种物质只含两种非金属元素,该物质中一定没有非极性供价键 | |
| D. | 氢键属于分子间作用力,不属于化学键 |
12.当下列物质以晶体形式存在时,其所属晶体类型和所含化学键类型分别相同的是( )
| A. | 氯化钠、氯化氢 | B. | 二氧化碳、二氧化硅 | ||
| C. | 四氯化碳、四氯化硅 | D. | 单质铁、单质碘 |
16.下列叙述正确的是( )
| A. | 常温常压下,4.6 g NO2气体约含有1.81×1023个原子 | |
| B. | 在标准状况下,80 gSO3所占的体积约为22.4L | |
| C. | 常温下,0.1 mol/L醋酸溶液的pH约为1 | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA |
6.设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有( )
| A. | 12g金刚石中含4NA个C-C共价键 | |
| B. | 2L 0.5 moI.L-1盐酸溶液所含的HCI分子数目为NA | |
| C. | 标准状况下,2.24LCL4含有的原子数为0.5NA | |
| D. | 7.1 gCL2与5.6 g Fe反应,转移的电子总数为0,2NA |
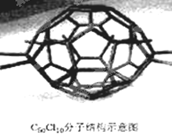
13.厦门大学郑兰荪院士合成了C70Cl10富勒烯足球状分子,如图,它是由C70分子与Cl2发生加成反应得到的.在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,70个碳原子组成若干个正六边形和正五边形.则有关说法中不正确的是
( )
( )

| A. | C70的熔点比石墨的熔点低 | |
| B. | C70和金刚石是同素异形体 | |
| C. | C70分子中含有70个σ键,35个π键 | |
| D. | C70Cl10分子中共用电子对数目为145个 |
10.在反应2SO2+18O2?2SO3中,其中氧气用18O标记上,其中含有18O的物质有( )
| A. | SO2 | B. | O2 SO3 | C. | SO2 O2 SO3 | D. | SO2 SO3 |
11.元素周期表中某区域可以寻找制备新型农药材料的元素,它们是( )
| A. | 左下方区域的金属元素 | |
| B. | 右上方区域的某些非金属元素 | |
| C. | 金属元素和非金属元素分界线附近的元素 | |
| D. | 过渡元素区域 |