4.填写下列表格(电解质溶液PH的变化一栏填写“变大”、“变小”或“不变”)
| 化学电源名称 | 正极反应式 | 负极反应式 | 电解质溶液pH的变化 |
| 碱性氢氧燃料电池 | O2+2H2O+4e-=4OH- | 此空不用填写 | 变小 |
| 碱性甲烷燃料电池 | 此空不用填写 | CH4+8e-+10OH-=CO32-+7H2O | 变小 |
2.相同条件下,下列各组中的两个反应的焓变前者大于后者的是( )
| A. | H2(g)+Cl2(g)=2HCl(g) 和H2(g)+Cl2(g)=2HCl(aq) | |
| B. | C2H4(g)+H2(g)=C2H6(g)和C3H6(g)+H2(g)=C3H8(g) | |
| C. | 2H2(g)+O2(g)=2H2O(l)和2H2(g)+O2(g)=2H2O(g) | |
| D. | C(s)+O2(g)=CO2(g)和C(s)+$\frac{1}{2}$O2(g)=CO(g) |
1.已知下列反应的焓变:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3KJ•mol-1
(2)C(s)+O2(g)=CO2(g)△H2=-393.5KJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H3=-285.8KJ•mol-1
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变为( )
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3KJ•mol-1
(2)C(s)+O2(g)=CO2(g)△H2=-393.5KJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H3=-285.8KJ•mol-1
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变为( )
| A. | -870.3KJ•mol-1 | B. | -571.6KJ•mol-1 | C. | +787.0KJ•mol-1 | D. | -488.3KJ•mol-1 |
20.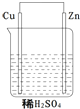 关于如图所示的原电池下列叙述正确的是( )
关于如图所示的原电池下列叙述正确的是( )
①电子由铜流向锌
②正极反应式为Cu+2e-=Cu2+
③SO42-向铜极移动
④铜电极上有气泡
⑤若有0.5mole-流经导线,则可产生0.25molH2
⑥烧杯中溶液的PH升高.
 关于如图所示的原电池下列叙述正确的是( )
关于如图所示的原电池下列叙述正确的是( )①电子由铜流向锌
②正极反应式为Cu+2e-=Cu2+
③SO42-向铜极移动
④铜电极上有气泡
⑤若有0.5mole-流经导线,则可产生0.25molH2
⑥烧杯中溶液的PH升高.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③⑤ | D. | ②④⑥ |
18.下列半径的比较中正确的是( )
| A. | Fe>Fe3+>Fe2+ | B. | Cl>S>P | C. | O2->Na+>Al3+ | D. | Ar>Kr>Xe |
17.用a、b、c、d四种金属进行如下图所示的实验,部分反应现象如下表所示,由此判断四种金属的活动性由强到弱的顺序是( )
0 168774 168782 168788 168792 168798 168800 168804 168810 168812 168818 168824 168828 168830 168834 168840 168842 168848 168852 168854 168858 168860 168864 168866 168868 168869 168870 168872 168873 168874 168876 168878 168882 168884 168888 168890 168894 168900 168902 168908 168912 168914 168918 168924 168930 168932 168938 168942 168944 168950 168954 168960 168968 203614
| 实验装置 | 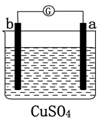 | 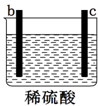 | 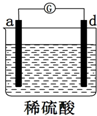 |
| 部分实验现象 | a极质量减少b极质量增加 | b极有气体产生c极无变化 | 电流从a极流向d极 |
| A. | abcd | B. | bcda | C. | dabc | D. | abdc |
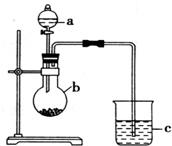 “元素的最高价氧化物对应的水化物酸性越强非金属性越强”某同学欲运用这一观点来验证硫和碳两元素的得电子的能力强弱,设计实验如图所示,请回答:
“元素的最高价氧化物对应的水化物酸性越强非金属性越强”某同学欲运用这一观点来验证硫和碳两元素的得电子的能力强弱,设计实验如图所示,请回答:


