15.已知:S(l)+O2(g)=SO2(g)△H=-293.23kJ•mol-1,分析下列说法中正确的是( )
| A. | S(s)+O2(g)=SO2(g),反应放出的热量大于293.23 kJ•mol-1 | |
| B. | S(g)+O2(g)=SO2(g),反应放出的热量小于293.23 kJ•mol-1 | |
| C. | 1 mol SO2(g)的键能的总和小于1 mol S(l)和1 mol O2(g)的键能之和 | |
| D. | 1 mol SO2(g)的键能的总和大于1 mol S(l)和1 mol O2(g)的键能之和 |
14.反应N2+3H2=2NH3的能量变化如图,其热化学方程式正确的是( )
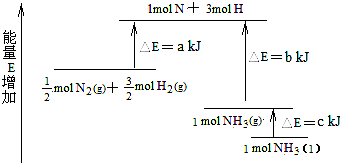
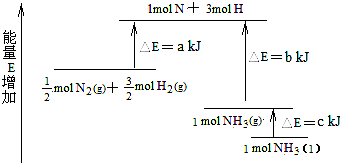
| A. | N2(g)+H2(g)=NH3(l)△H=+(b+c-a)kJ•mol-1 | |
| B. | N2(g)+3H2(g)=2NH3(g)△H=+2(b-a)kJ•mol-1 | |
| C. | N2(g)+3H2(g)=2NH3(l)△H=-2(b+c-a)kJ•mol-1 | |
| D. | N2(g)+H2(g)=NH3(g)△H=+(a+b)kJ•mol-1 |
13.已知Fe(s)+H2SO4(aq)=FeSO4(aq)+H2(g)△H<0,则下列关于该反应的叙述不正确的是( )
| A. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| B. | 上述热化学方程式中的△H的值与反应物的用量有关 | |
| C. | 该反应的化学能可以转化为电能 | |
| D. | 此反应构成的原电池中,正极可以是碳棒、铜或锌 |
12.下列物质中含有共价键的离子化合物是( )
| A. | BaCl2 | B. | H2O | C. | HCl | D. | Ba(OH)2 |
11.某元素原子的原子核外有三个电子层,最外层上的电子数是另外两个电子层电子数之差,该原子核内质子数为( )
| A. | 18 | B. | 16 | C. | 8 | D. | 6 |
10.元素的性质呈周期性变化的根本原因是( )
| A. | 元素的相对原子质量呈周期性变化 | |
| B. | 元素的原子半径呈周期性变化 | |
| C. | 元素的金属性和非金属性呈周期性变化 | |
| D. | 元素原子的核外电子排布呈周期性变化 |
9.某溶液中只含有K+、Fe3+、NO3-,已知K+、Fe3+的个数分别为3a和a,则溶液中K+与NO3-的个数比为( )
| A. | 1:4 | B. | 1:2 | C. | 3:4 | D. | 3:2 |
8.向物质M的溶液中逐滴加入NaOH溶液,先产生白色沉淀,然后沉淀逐渐溶解,则物质M可能是( )
| A. | MgSO4 | B. | FeCl2 | C. | AlCl3 | D. | NaAlO2 |
7.下列说法均摘自某些科普杂志,你认为无科学性错误的是( )
0 166964 166972 166978 166982 166988 166990 166994 167000 167002 167008 167014 167018 167020 167024 167030 167032 167038 167042 167044 167048 167050 167054 167056 167058 167059 167060 167062 167063 167064 167066 167068 167072 167074 167078 167080 167084 167090 167092 167098 167102 167104 167108 167114 167120 167122 167128 167132 167134 167140 167144 167150 167158 203614
| A. | 铅笔芯的原料是重金属铅,儿童在使用时不可以用嘴吮吸铅笔,以免引起铅中毒 | |
| B. | CO有毒,生有煤炉的居室放置数盆清水,这样可有效的吸收CO,防止煤气中毒 | |
| C. | 汽水浇灌农田有一定的道理,其中二氧化碳的缓释,有利于作物的光合作用 | |
| D. | 纯碱又名烧碱,成分是氢氧化钠 |
