18.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 12g金刚石晶体中含有的C-C的数目为2NA | |
| B. | 1L1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 5.6gFe与足量的水蒸气完全反应,转移电子的数目为0.2NA | |
| D. | 标准状况下,22gCO2气体中含有的σ键和π键的数目均为2NA |
17.下列有关叙述错误的是( )
| A. | 推广使用无磷洗衣粉主要是为了防止水体富营养化 | |
| B. | 高铁酸钾(K2FeO4)是一种新型自来水处理剂,有强氧化性可消毒杀菌,其还原产物能吸附水中杂质 | |
| C. | 石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 | |
| D. | 测定有机物结构方法较多,如红外光谱、紫外光谱、质谱、核磁共振氢谱、同位素原子示踪法等 |
12.已知25℃时,电离常数Ka(HF)=3.6×10-4mol•L-1,溶度积常数Ksp(CaF2)=1.46×10-10,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.O×10一16.下列说法正确的是( )
| A. | 25℃时,O.1 mol•L-1HF溶液pH=l,Ksp(CaF2)随温度和浓度的变化而变化 | |
| B. | 向1L0.2 mol•L-1HF溶液中加入1L O.2 mol•L-1CaCl2溶液,没有沉淀产生 | |
| C. | AgCl不溶于水,不能转化为AgI | |
| D. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于$\frac{1}{\sqrt{1.8}}$×10-11mol•L-1 |
11. 日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )
日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )
 日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )
日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )| A. | a极为电池的负极 | |
| B. | A-为OH- | |
| C. | 电池充电时阴极反应为:LiCn+e-═Li++nC | |
| D. | 充电时,溶液中A-从b极向a极迁移 |
10.下列图示实验正确的是( )
| A. | 测量Cu与浓硝酸反应产生气体的体积: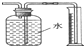 | |
| B. | 验证Na和水反应为放热反应: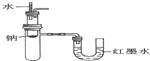 | |
| C. | 制取干燥的氨气: | |
| D. | 收集H2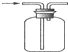 |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
0 166868 166876 166882 166886 166892 166894 166898 166904 166906 166912 166918 166922 166924 166928 166934 166936 166942 166946 166948 166952 166954 166958 166960 166962 166963 166964 166966 166967 166968 166970 166972 166976 166978 166982 166984 166988 166994 166996 167002 167006 167008 167012 167018 167024 167026 167032 167036 167038 167044 167048 167054 167062 203614
| A. | 标准状况下,18 g H20所含的中子数为10NA | |
| B. | 一定条件下1 mol铁粉与浓硫酸反应,转移电子数一定为3NA | |
| C. | 在1 L的碳酸钠溶液中,若c(CO32一)=1 mol•L-1,则Na+数目大于2NA | |
| D. | 含阴阳离子总数为4NA的固体Na202溶于水配成1 L溶液,所得溶液中Na+的物质的量浓度为2 mol•L-1 |
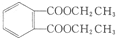 )是一种重要的工业塑化剂,其合成路线很多,如图就是其中的一种合成方法:
)是一种重要的工业塑化剂,其合成路线很多,如图就是其中的一种合成方法: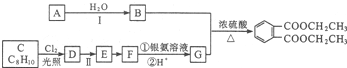
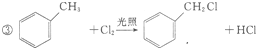
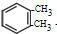 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$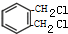 +2HCl.
+2HCl.
 亚硝酸(HN02)在工业上用于有机合成,既具有氧化性又具有还原性,而且氧化性比还原性突出得多.回答下列问题:
亚硝酸(HN02)在工业上用于有机合成,既具有氧化性又具有还原性,而且氧化性比还原性突出得多.回答下列问题: