5.X、Y、Z、W是短周期元素,原子序数依次增大.X是原子半径最小的元素;Y元素原子的最外层电子数是电子层数的2倍;Z元素的-1价阴离子、W元素的+3价阳离子的核外电子排布均与氖原子相同.下列说法正确的是( )
| A. | X、Y形成的具有10e-的分子中含非极性共价键 | |
| B. | X单质和Z单质在暗处剧烈反应形成的化合物比HCl稳定 | |
| C. | 含W元素的盐溶液一定显酸性 | |
| D. | Z离子半径小于W离子半径 |
4.下列实验现象不能说明相关结论的是( )
| A. | 向Al(OH)3沉淀滴加NaOH或盐酸沉淀均消失,说明Al(OH)3是两性氢氧化物 | |
| B. | 饱和Na2S溶液中滴入少量氯水出现浑浊,说明元素非金属性Cl>S | |
| C. | 将铜丝插入锌粒与稀硫酸反应体系中反应明显加快,原因是形成了原电池 | |
| D. | 饱和食盐水中滴入浓硫酸析出食盐晶体,说明浓硫酸吸水放出大量的热 |
3.一定条件下(恒温、恒容的密闭容器中)合成氨反应处于化学平衡状态的是( )
| A. | υ(N2生成)=3υ(H2消耗) | |
| B. | H2、H2、HN3的分子数之比为1:3:2 | |
| C. | 单位时间内生成2molNH3,同时消耗1molH2 | |
| D. | 容器内的压强不再变化 |
2.H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g),1molH2完全反应放出akJ热量.
已知:
 (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
已知:
 (a、b、c均大于零)
(a、b、c均大于零)下列说法不正确的是( )
| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1molH-H键和1molI-I键所需能量大于断开2molH-I键所需能量 | |
| C. | 断开2molH-I键所需能量约为(c+b+a)kJ | |
| D. | 向密闭容器中加入2molH2和2molI2,充分反应放出的热量大小2akJ |
1.如图是元素周期表的一部分,下列关系正确的是( )
| S | Cl |
| Se | Br |
| A. | 还原性:Se2->S2->Cl- | B. | 热稳定性:HCl>H2Se>HBr | ||
| C. | 原子半径:Se>Cl>S | D. | 酸性:HBrO4>HClO4>H2SeO4 |
20.氮氧化铝(AlON)是一种高硬度防弹材料,可以在高温下由反应Al2O3+C+N2═2AlON+CO合成,下列有关说法合理的是( )
| A. | 上述反应中氮气作还原剂 | |
| B. | 氮氧化铝中氮元素的化合价是-3 | |
| C. | 氮氧化铝晶体中的作用力是范德华力 | |
| D. | 根据氮氧化铝晶体的硬度可推断其晶体类型可能与石英相同 |
19.向一定量Fe、FeO、Fe2O3的混合物中,加入50mL1mol•L-1硫酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现.若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量为( )
| A. | 11.2g | B. | 2.8g | C. | 5.62g | D. | 无法计算 |
18.下列操作不正确的是( )
| A. | 用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率 | |
| B. | 含不溶性杂质的粗苯甲酸进行重结晶分离的操作步骤之一是趁热过滤 | |
| C. | 做银镜反应实验后,用硝酸洗涤试管壁上的银镜 | |
| D. | 制备乙酸乙酯时,先向大试管中加入浓硫酸,再逐滴加入乙醇和乙酸 |
17.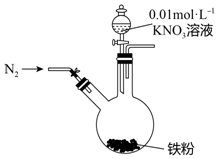 某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验步骤及现象如下:
某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验步骤及现象如下:
(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是防止空气中的O2对Fe和NO3-反应的干扰,避免影响反应产物的判断.
(2)白色物质是Fe(OH)2,用化学方程式解释其变为红褐色的原因:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(3)为了探宄滤液的成分,该同学进一步设计了下述实验:
(i)根据以上实验现象,可以判断滤液中存在NH4+、Fe2+、NO3-离子.
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
 某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验步骤及现象如下:
某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验步骤及现象如下:| 实验步骤 | 实验现象 |
| 1.打开弹簧夹,缓慢通入N2 | |
| 2.加入pH为2.5的0.01mol/L酸性KNO3溶液100mL | 铁粉部分溶解,溶液呈浅绿色; 铁粉不再溶解后,剩余铁粉表面出现少量白色物质附着. |
| 3.反应停止后,拔掉橡胶塞,将圆底烧瓶取下 | 烧瓶内气体的颜色没有发生变化. |
| 4将剩余固体过滤 | 表面的白色物质变为红褐色. |
(2)白色物质是Fe(OH)2,用化学方程式解释其变为红褐色的原因:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(3)为了探宄滤液的成分,该同学进一步设计了下述实验:
| 实验步骤 | 实验现象 |
| 1.取部分滤液于试管中,向其中加入KSCN溶液 | 溶液液无变化 |
| 2.将上述溶液分为两份,一份中滴入氯气;另一份中滴加稀硫酸 | 两份溶液均变为红色 |
| 3.另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸. | 有气体生成,该气体使红色石蕊试纸变蓝. |
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
16.下列有关钢铁腐蚀与防护和说法错误的是( )
0 163912 163920 163926 163930 163936 163938 163942 163948 163950 163956 163962 163966 163968 163972 163978 163980 163986 163990 163992 163996 163998 164002 164004 164006 164007 164008 164010 164011 164012 164014 164016 164020 164022 164026 164028 164032 164038 164040 164046 164050 164052 164056 164062 164068 164070 164076 164080 164082 164088 164092 164098 164106 203614
| A. | 当镀层都被破坏时,镀锌铁比镀锡铁更易被锈蚀 | |
| B. | 钢铁发生析氢腐蚀时和吸氧腐蚀时负极反应均是Fe-2e-=Fe2+ | |
| C. | 钢铁闸门上装上锌块是利用牺牲阳极的阴极保护法来防止其被腐蚀 | |
| D. | 钢管与电源负极连接是利用外加电流的阴极保护法来防止其被腐蚀 |