5.利用铝热反应原理焊接钢轨的化学方程式为Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,关于该反应的叙述错误的是( )
| A. | 属于置换反应 | B. | A1作还原剂 | ||
| C. | Fe2O3被还原 | D. | 该反应是吸热反应 |
3.容积相同的四个密闭容器中,进行同样的可逆反应:2A(g)+B(g)?3C(g)+2D(g);起始时甲、乙、丙、丁四个容器所装A和B的量分别为:
甲:A 2mol,B 1mol; 乙:A 1mol,B 1mol; 丙:A 2mol,B 2mol;丁:A 1mol,B 2mol.在相同温度下建立平衡时,A或B的转化率大小关系为( )
甲:A 2mol,B 1mol; 乙:A 1mol,B 1mol; 丙:A 2mol,B 2mol;丁:A 1mol,B 2mol.在相同温度下建立平衡时,A或B的转化率大小关系为( )
| A. | A的转化率为甲<丙<乙<丁 | B. | A的转化率为甲<乙<丁<丙 | ||
| C. | B的转化率为甲>乙>丙>丁 | D. | B的转化率为甲<丙<乙<丁 |
2.N2O5是一种新型绿色硝化剂.用硼氢化钠(NaBH4)燃料电池做电源,电解法制备N2O5的装置简图如下(隔膜只允许H+ 通过).

回答下列问题:
(1)电池负极反应式是BH4-+8OH--8e-=BO2-+6H2O,电解池阳极生成N2O5的电极反应式是N2O4+2HNO3-2e-=2N2O5+2H+.
(2)隔膜不允许水分子通过的原因是H2O 通过隔膜进入阳极,与N2O5反应生成HNO3.N2O5在一定温度下可发生分解反应:2N2O5 (g)?2N2O4(g)+O2(g)△H>0,t℃时,向一定容积的密闭容器中通入N2O5(g),部分实验数据见下表:
(3)500s 时,c(O2)=1.375 mol?L-1.
(4)t℃时,该反应平衡常数K值为1.25.
(5)下列措施能降低N2O5分解率的是③④⑤.
①升温 ②通入N2 ③通入O2 ④通入N2O5 ⑤NO2.

回答下列问题:
(1)电池负极反应式是BH4-+8OH--8e-=BO2-+6H2O,电解池阳极生成N2O5的电极反应式是N2O4+2HNO3-2e-=2N2O5+2H+.
(2)隔膜不允许水分子通过的原因是H2O 通过隔膜进入阳极,与N2O5反应生成HNO3.N2O5在一定温度下可发生分解反应:2N2O5 (g)?2N2O4(g)+O2(g)△H>0,t℃时,向一定容积的密闭容器中通入N2O5(g),部分实验数据见下表:
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol•L-1 | 5.00 | 2.25 | 2.50 | 2.50 |
(4)t℃时,该反应平衡常数K值为1.25.
(5)下列措施能降低N2O5分解率的是③④⑤.
①升温 ②通入N2 ③通入O2 ④通入N2O5 ⑤NO2.
18.分子式为C3H6Cl2的有机物,发生一元氯代反应后,可以生成三种同分异构体,则原C3H6Cl2的名称是( )
| A. | 1,2-二氯丙烷 | B. | 1,1-二氯丙烷 | C. | 1,3-二氯丙烷 | D. | 2,2-二氯丙烷 |
17.有3LCH4与CO、H2的混合气体,在10LO2中完全燃烧后,测得气体的体积为12.5L(气体体积均在120℃1.01×105Pa下测定),则原气体中CH4的体积为( )
| A. | 3L | B. | 2L | C. | 1L | D. | 无法确定 |
16.几种短周期元素的原子半径及主要化合价见表:
下列叙述正确的是( )
0 163904 163912 163918 163922 163928 163930 163934 163940 163942 163948 163954 163958 163960 163964 163970 163972 163978 163982 163984 163988 163990 163994 163996 163998 163999 164000 164002 164003 164004 164006 164008 164012 164014 164018 164020 164024 164030 164032 164038 164042 164044 164048 164054 164060 164062 164068 164072 164074 164080 164084 164090 164098 203614
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | 氢化物的沸点Q>T | |
| B. | M与T形成的化合物有两性 | |
| C. | L、R的单质与稀盐酸反应速率L<R | |
| D. | L、Q形成的简单离子核外电子数相等 |
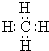 ,AxByCz的分子式AlC3H9.
,AxByCz的分子式AlC3H9.