20.一定温度下,溴化银在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )

| A. | 向溴化银悬浊液中加入溴化钠溶液,溴化银的Ksp减小 | |
| B. | 图中a点对应的是不饱和溶液 | |
| C. | 向c点对应的溶液中加入少量0.1 mol•L-1 AgNO3溶液,则c(Br-)增大 | |
| D. | 升高温度可以实现c点对应的溶液到b点对应的溶液的转化 |
19. 常温下,向l0mL0.1mol/L的HR溶液中逐渐滴入0.lmol/L的NH3•H2O 溶液,所得溶液pH及导电性变化如图.下列分析不正确的是( )
常温下,向l0mL0.1mol/L的HR溶液中逐渐滴入0.lmol/L的NH3•H2O 溶液,所得溶液pH及导电性变化如图.下列分析不正确的是( )
 常温下,向l0mL0.1mol/L的HR溶液中逐渐滴入0.lmol/L的NH3•H2O 溶液,所得溶液pH及导电性变化如图.下列分析不正确的是( )
常温下,向l0mL0.1mol/L的HR溶液中逐渐滴入0.lmol/L的NH3•H2O 溶液,所得溶液pH及导电性变化如图.下列分析不正确的是( )| A. | a〜b点导电能力增强,说明HR为弱酸 | |
| B. | b点溶液,c(NH3•H2O)=c(R-)+c(H+)-c(OH-) | |
| C. | c点溶液,存在c(NH4+)>c(R-)>c(OH-)>c(H+) | |
| D. | 常温下,HR和NH3•H2O的电离平衡常数相等 |
18. 25℃时,向盛有50mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )
25℃时,向盛有50mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )
 25℃时,向盛有50mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )
25℃时,向盛有50mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )| A. | HA溶液的物质的量浓度为0.0l mol/L | |
| B. | a→b的过程中,混合溶液不可能存在:c(A-)=c(Na+) | |
| C. | b→c的过程中,温度降低的主要原因是溶液中A-发生了水解反应 | |
| D. | 25℃时,HA的电离平衡常数K约为1.25×10-6 |
15.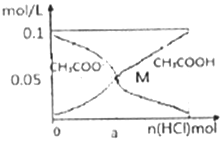 常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
 常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )| A. | 当n(HCl)=1.0×10-3mol时,溶液中 c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) | |
| B. | M点溶液中水的电离程度比原溶液小 | |
| C. | 随着HCl的通入,c(OH-)/c(CH3COO-) 值不断减小 | |
| D. | 在M 点时,c(H+)-c(OH-)=(a-0.05)mol/L |
14.通常把原子总数和价电子总数相同的分子或离子称为等电子体.人们发现等电子体的 空间结构相同,则下列有关说法中正确的是( )
| A. | CH${\;}_{4}^{-}$和 NH${\;}_{4}^{+}$是等电子体,键角均为 60° | |
| B. | NO${\;}_{3}^{-}$和 CO${\;}_{3}^{2-}$是等电子体,都是平面三角形结构 | |
| C. | H3O和 PCl3是等电子体,均为三角锥形结构 | |
| D. | B3N3H6 和苯是等电子体,B3N3 H6 分子中也存在“肩并肩”式重叠的轨道 |
13. 常温下用0.100 0mol•L-1的盐酸分别逐滴加入到20.00mL 0.100 0mol•L-1的三种一元碱MOH、XOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示.下列说法正确的是( )
常温下用0.100 0mol•L-1的盐酸分别逐滴加入到20.00mL 0.100 0mol•L-1的三种一元碱MOH、XOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示.下列说法正确的是( )
0 163661 163669 163675 163679 163685 163687 163691 163697 163699 163705 163711 163715 163717 163721 163727 163729 163735 163739 163741 163745 163747 163751 163753 163755 163756 163757 163759 163760 163761 163763 163765 163769 163771 163775 163777 163781 163787 163789 163795 163799 163801 163805 163811 163817 163819 163825 163829 163831 163837 163841 163847 163855 203614
 常温下用0.100 0mol•L-1的盐酸分别逐滴加入到20.00mL 0.100 0mol•L-1的三种一元碱MOH、XOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示.下列说法正确的是( )
常温下用0.100 0mol•L-1的盐酸分别逐滴加入到20.00mL 0.100 0mol•L-1的三种一元碱MOH、XOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示.下列说法正确的是( )| A. | 分别加入盐酸10 mL时:c(X+)>c(M+)>c(Y+)>c(Cl-) | |
| B. | 分别加入盐酸15 mL时:c(Cl-)>c(X+)>c(MOH)>c(YOH) | |
| C. | 分别加入盐酸至pH=7时:c(X+)=c(M+)=c(Y+) | |
| D. | 将分别加入盐酸20 mL后的三种溶液混合:c(H+)+c(Y+)=c(OH-)+c(X+)+c(MOH) |
 .
.