题目内容
20.一定温度下,溴化银在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
| A. | 向溴化银悬浊液中加入溴化钠溶液,溴化银的Ksp减小 | |
| B. | 图中a点对应的是不饱和溶液 | |
| C. | 向c点对应的溶液中加入少量0.1 mol•L-1 AgNO3溶液,则c(Br-)增大 | |
| D. | 升高温度可以实现c点对应的溶液到b点对应的溶液的转化 |
分析 A.溶度积常数只与温度有关;
B.根据c(Ag+)×c(Br-)与Ksp的相对大小判断溶液是否是饱和溶液,如果c(Ag+)×c(Br-)=Ksp,则溶液为平衡状态,如果c(Ag+)×c(Br-)>Ksp,则溶液为过饱和溶液,如果c(Ag+)×c(Br-)<Ksp,则溶液为不饱和溶液;
C.根据浓度对溶解平衡的影响判断;
D.升高温度,促进溶解平衡正向移动.
解答 解:A.溶液的温度不变,所以Ksp不变,故A错误;
B.a点c(Ag+)×c(Br-)<Ksp,则溶液为不饱和溶液,故B正确;
C.向c点的溶液中加入0.1mol•L-1AgNO3,c(Ag+)增大,溶解平衡逆向移动,则c(Br-)减小,故C错误;
D.升高温度,促进溴化银的溶解,c(Ag+)、c(Br-)浓度都增大,故D错误;
故选B.
点评 本题考查难溶电解质的溶解平衡问题,为高频考点,侧重考查学生的分析能力,题目难度中等,注意把握题给图象曲线的意义,明确溶度积常数只与温度有关,与溶液的浓度无关.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列说法中正确的是( )
| A. | 用分液漏斗分离硬脂酸钠与甘油的混合物 | |
| B. | 容量瓶用蒸馏水洗涤后须烘干才能使用 | |
| C. | 分馏石油时,温度计的水银球必须插入液面以下 | |
| D. | 氯化钠溶液蒸发结晶时,蒸发皿中有大量晶体析出并剩余少量溶液时应停止加热 |
13.等温等压下,有质子数相等的CO、N2、C2H2三种气体.下列说法正确的是( )
| A. | 质量之比为1:1:1 | B. | 体积之比为4:14:13 | ||
| C. | 密度之比为13:13:14 | D. | 原子个数之比为1:1:2 |
8. 连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )
连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )
 连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )
连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )| A. | H2N2O2在水溶液中的电离方程式为H2N2O2═2H++N2O22- | |
| B. | 该滴定过程应该选择甲基橙作为指示剂 | |
| C. | a点的溶液中:c(Na+)+c(H+)═c(OH-)+c(N2O22-)+c(H N2O2-) | |
| D. | b点的溶液中:c(Na+)>c(H N2O2-)>c(OH-)>c(H2N2O2)>c(N2O22-) |
15.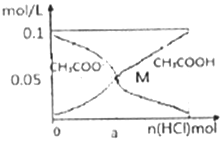 常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
 常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )| A. | 当n(HCl)=1.0×10-3mol时,溶液中 c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) | |
| B. | M点溶液中水的电离程度比原溶液小 | |
| C. | 随着HCl的通入,c(OH-)/c(CH3COO-) 值不断减小 | |
| D. | 在M 点时,c(H+)-c(OH-)=(a-0.05)mol/L |
5.下列物质不属于高分子化合物的是( )
| A. | 聚乙烯塑料 | B. | 酶 | C. | 油脂 | D. | 淀粉 |
12.下列关于有机物因果关系的叙述中,完全正确的一组是( )
| 选项 | 原因 | 结论 |
| A | 乙烯和苯都能使溴水褪色 | 苯和乙烯分子都含有碳碳双键 |
| B | 乙酸乙酯和乙烯一定条件下都能和水反应 | 两者属于同一类型的反应 |
| C | 乙酸、葡萄糖都能与新制的氢氧化铜反应 | 都同属于氧化反应 |
| D | 乙烯能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色 | 两者的褪色本质是不相同的 |
| A. | A | B. | B | C. | C | D. | D |
9.可以证明次氯酸是弱酸的事实是( )
| A. | 可与碱发生反应 | B. | 有漂白性 | ||
| C. | 次氯酸钠与碳酸反应有次氯酸生成 | D. | 见光能分解 |
10.下列实验能达到预期目的是( )
| A. | 用分液漏斗分离溴和苯 | |
| B. | 分馏石油时,将温度计插入石油液面下 | |
| C. | 取样灼烧,可以鉴别白色纺织品是棉织品还是羊毛制品 | |
| D. | 直接往淀粉水解液中加入新制氢氧化铜悬浊液并且加热,可检验淀粉水解产物 |