19.下列关于苯的说法正确的是( )
| A. | 能与水互溶 | B. | 密度比水大 | ||
| C. | 能发生取代反应 | D. | 分子中存在单双键结构 |
18.某元素的最高正价与负价的代数和为4,则该元素可能为( )
| A. | C | B. | P | C. | O | D. | S |
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,2.24L戊烷所含分子数为0.1 NA | |
| B. | 78gNa2O2固体与足量的H2O反应转移的电子数为0.5NA | |
| C. | 17.6g丙烷中所含的极性共价键为4NA个 | |
| D. | 2.0gH218O和D216O的混合物中所含中子数为NA |
16.将0.4molSO2和0.2molO2置于密闭容器中发生反应:2SO2+O2$?_{催化剂}^{高温}$2SO3.下列关于该反应的说法正确的是( )
| A. | 最终可生成0.4molSO3 | |
| B. | 当v正(O2)=v逆(SO2)=0时一定达化学平衡 | |
| C. | 升高温度反应速率减小 | |
| D. | 缩小体积增大压强反应速率增大 |
15.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: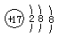 | |
| B. | CH4的球棍模型:? | |
| C. | 氯化镁的电子式: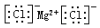 | |
| D. | 硫酸的电离方程式:H2SO4═H2++SO42ˉ |
14.在恒温密闭容器中发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),以下可以证明该反应已达平衡状态的是( )
| A. | 3v正(H2)=v逆(CH3OH) | B. | 混合气体的密度不再改变 | ||
| C. | 容器内压强不再改变 | D. | 反应物与生成物的浓度相等 |
13.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 电解CuCl2溶液,阴极析出16g铜时,电极上转移的电子数为NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有C-C键的个数为4NA | |
| D. | SiO2晶体中每摩尔硅原子可与氧原子形成2NA个共价键 |
12.下列分子中的中心原子杂化轨道的类型相同的是( )
| A. | CO2与SO2 | B. | CH4与NH3 | C. | BeCl2与BF3 | D. | C2H4与C2H2 |
11.设阿伏加德罗常数为NA,则下列说法正确的是( )
0 163508 163516 163522 163526 163532 163534 163538 163544 163546 163552 163558 163562 163564 163568 163574 163576 163582 163586 163588 163592 163594 163598 163600 163602 163603 163604 163606 163607 163608 163610 163612 163616 163618 163622 163624 163628 163634 163636 163642 163646 163648 163652 163658 163664 163666 163672 163676 163678 163684 163688 163694 163702 203614
| A. | 常温常压下,11.2 L甲烷中含有的氢原子数为2NA | |
| B. | 标准状况下,0.3 mol二氧化硫中含有的氧原子数为0.3NA | |
| C. | 常温下,2.7 g Al与足量的盐酸反应,生成H2的分子数为0.15NA | |
| D. | 常温下,0.1 mol•L-1MgCl2溶液中含Cl-数为0.2NA |




 .
.