17.如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )


| A. | ZM2分子中各原子的最外层均满足8电子稳定结构 | |
| B. | 离子半径:M->Z2->Y- | |
| C. | 电负性:Y>Z>M | |
| D. | Z元素基态原子最外层电子排布图为: |
16.下列物质,按沸点降低顺序排列的一组是( )
| A. | HF、HCl、HBr、HI | B. | F2、Cl2、Br2、I2 | ||
| C. | H2O、H2S、H2Se、H2Te | D. | CI4、CBr4、CCl4、CF4 |
13.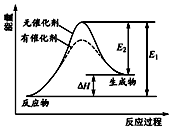 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 催化剂能降低反应的活化能 | |
| C. | 该反应的△H=E2-E1 | |
| D. | 该图可以表示燃料燃烧反应的能量变化 |
11.下列反应中,属于吸热反应的是( )
| A. | Na与H2O反应 | B. | H2在Cl2中燃烧 | ||
| C. | NaOH溶液与盐酸反应 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
10.下列物质中,只含离子键的是( )
| A. | H2 | B. | NH3 | C. | MgCl2 | D. | NaOH |
9.已知反应2I-+S2O82-═I2+2SO42-,加入淀粉溶液可观察到溶液变蓝色.反应速率可以用淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.20℃时得到如下实验数据:
分析上述数据,下列说法正确的是( )
| 实验编号 | C(I-)/mol•L | C(S2O82-)/mol•L | t/s |
| 1 | 0.040 | 0.040 | 88.0 |
| 2 | 0.080 | 0.040 | 44.0 |
| 3 | 0.080 | 0.080 | 22.0 |
| 4 | 0.160 | 0.020 | 44.0 |
| 5 | 0.120 | 0.040 | 29.3 |
| A. | I-的浓度越大,反应速率越快 | |
| B. | S2O82- 的浓度越大,反应速率越快 | |
| C. | 该实验的目的是研究 I- 与S2O82- 的浓度对反应速率的影响 | |
| D. | 5个实验中,编号3对应浓度的实验,反应速率最慢 |
8.设阿伏加德罗常数为NA,下列说法中正确的是(Mg-24 H-1 O-16)( )
0 163368 163376 163382 163386 163392 163394 163398 163404 163406 163412 163418 163422 163424 163428 163434 163436 163442 163446 163448 163452 163454 163458 163460 163462 163463 163464 163466 163467 163468 163470 163472 163476 163478 163482 163484 163488 163494 163496 163502 163506 163508 163512 163518 163524 163526 163532 163536 163538 163544 163548 163554 163562 203614
| A. | 18g H2O含有的电子数8NA | |
| B. | 常温常压下,1L0.2mol/L MgCl2溶液中含Cl-数为0.2NA | |
| C. | 常温常压下,22.4L的氧气中含氧原子数为2NA | |
| D. | 2.4g的Mg粉与足量的盐酸反应失去电子数为0.2NA |
 科学家参考自然界中的光合作用,设计利用太阳能促进燃料的循环使用(如图),其中过程Ⅰ的主要反应如下:
科学家参考自然界中的光合作用,设计利用太阳能促进燃料的循环使用(如图),其中过程Ⅰ的主要反应如下: 如图为氢氧燃料电池装置示意图.
如图为氢氧燃料电池装置示意图.