5.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 用石墨作电极电解饱和食盐水时,若阴极得到2 NA个电子,则阳极产生22.4 L气体 | |
| B. | 2 L 0.05 mol•L-1乙酸溶液中H+数目为0.1 NA | |
| C. | 足量的Cu与含有0.2 mol H2SO4的浓硫酸共热可生成SO2为0.1 NA | |
| D. | 7.8 g Na2S 和Na2O2的混合物中,含有的阴离子数目为0.1 NA |
4.实验室模拟从海水中制备NaOH溶液,其流程如下:

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 步骤一用到的仪器有坩埚、三脚架和泥三角 | |
| B. | 步骤二添加NaOH的目的是除去Ca2+ | |
| C. | 步骤二的过滤操作是在加入盐酸之后 | |
| D. | 步骤三最后一步反应为2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑ |
3.江西某铜业公司在火法炼铜时也生产硫酸,硫酸车间如图.下列叙述不正确的是( )


| A. | 自然界化合态硫主要以硫铁矿、黄铜矿、石膏、芒硝等形式存在 | |
| B. | 火法炼铜的矿石原料主要含CuS | |
| C. | 该公司炼铜产生的SO2可用于生产H2SO4 | |
| D. | 常温下,18.4 mol/L H2SO4溶液可储存于铁制或铝制容器 |
2. X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期.下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物.下列分析正确的是( )
X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期.下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物.下列分析正确的是( )
 X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期.下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物.下列分析正确的是( )
X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期.下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物.下列分析正确的是( )| A. | 离子半径:Y>Z | B. | Z的含氧酸均有强氧化性 | ||
| C. | 与Y同周期氢化物中D最稳定 | D. | F含离子键和共价键 |
1.下列有关化学用语表示正确的是( )
| A. | CSO的电子式: | |
| B. | Cl-的结构示意图: | |
| C. | 原子核内有20个中子的氯原子:${\;}_{17}^{20}$Cl | |
| D. | 苯分子的球棍模型: |
20. 常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )
常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )
 常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )
常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )| A. | 该Na2CO3溶液的浓度为0.001mol/L | |
| B. | 在pH=7时,c(Na+)>c(Cl-) | |
| C. | 在pH=6时,c(Na+)>c(CO32-)>c(HCO3-) | |
| D. | c→d发生的主要离子反应为:CO32-+H+=HCO3- |
18.图是某酸性酒精检测仪的工作示意图.下列有关分析正确的是( )


| A. | 该检测仪利用了电解原理 | |
| B. | 质子交换膜具有类似盐桥的平衡电荷作用 | |
| C. | Pt(l)极反应为:CH3CH2OH-4e-+H2O=4H++CH3COOH | |
| D. | 工作中电子由Pt(l)电极经过质子交换膜流向Pt(II) |
17.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
0 163121 163129 163135 163139 163145 163147 163151 163157 163159 163165 163171 163175 163177 163181 163187 163189 163195 163199 163201 163205 163207 163211 163213 163215 163216 163217 163219 163220 163221 163223 163225 163229 163231 163235 163237 163241 163247 163249 163255 163259 163261 163265 163271 163277 163279 163285 163289 163291 163297 163301 163307 163315 203614
| A. | 在25℃、1.01×105 Pa时,11.2 L氮气所含的原子数目为NA | |
| B. | 常温下,1 L 0.1 mol/L的Na2CO3溶液中含有的离子总数为0.3 NA | |
| C. | 钠在空气中燃烧可生成多种氧化物,23 g钠充分燃烧时转移电子数为1 NA | |
| D. | 1 mol P4和1 mol CH4中含有的共价健数均为4 NA |
 据图回答下列问题:
据图回答下列问题:
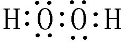 ,用电子式表示Y的形成过程
,用电子式表示Y的形成过程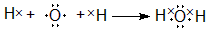 ;
;