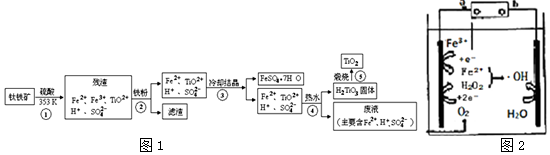
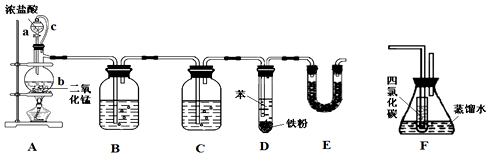
20.氯苯在染料、医药工业中有广泛的应用,某实验小组利用如图装置合成氯苯(支撑用的铁架台部分省略)并通过一定操作提纯氯苯.
反应物和产物的相关数据列表如下:
请按要求回答下列问题.
(1)装置A中橡胶管c的作用是,装置E的作用是除去氯气和氯化氢气体,防止大气污染.
(2)实验时;使a中的浓盐酸缓缓滴下,可观察到仪器b内的现象是有黄绿色气体生成,写出反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(3)为证明氯气和苯发生的是取代而不是加成反应,该小组用装置F说明,则装置F置于D和E之间(填字母),F中小试管内CCl4的作用是除去氯气,还需使用的试剂是硝酸酸化的硝酸银溶液.
(4)已知D中加入5mL苯,经过提纯后收集到氯苯3.0g,则氯苯的产率为47.3%(保留三位有效数字).

反应物和产物的相关数据列表如下:
| 密度/g•cm-3 | 沸点/℃ | 水中溶解性 | |
| 苯 | 0.879 | 80.1 | 微溶 |
| 氯苯 | 1.11 | 131.7 | 不溶 |
(1)装置A中橡胶管c的作用是,装置E的作用是除去氯气和氯化氢气体,防止大气污染.
(2)实验时;使a中的浓盐酸缓缓滴下,可观察到仪器b内的现象是有黄绿色气体生成,写出反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(3)为证明氯气和苯发生的是取代而不是加成反应,该小组用装置F说明,则装置F置于D和E之间(填字母),F中小试管内CCl4的作用是除去氯气,还需使用的试剂是硝酸酸化的硝酸银溶液.
(4)已知D中加入5mL苯,经过提纯后收集到氯苯3.0g,则氯苯的产率为47.3%(保留三位有效数字).
19.下列有关说法正确的是( )
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 古代做衣服的主要原料麻,其主要成分可表示为(C6H12O6)n | |
| C. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| D. | 食盐中含适量的碘酸钾,食用后可有效地抗核辐射 |
18.闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质.软锰矿的主要成分为 MnO2;含少量A12O3和SiO2.现以闪锌矿和软猛矿为原料制备Zn和MnO2,其简化流程如图1(中间产物的固体部分已经略去).
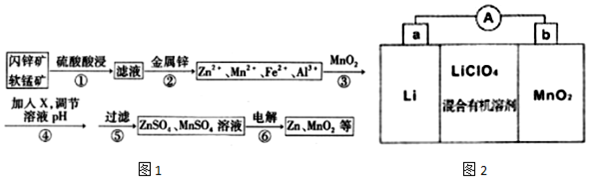
已知:I.矿石中所有金属元素在滤液中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
回答下列问题:
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式3MnO2+2FeS+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$3MnSO4+Fe2(SO4)3+2S+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③与MnO2发生氧化还原反应的离子方程式MnO2+2Fe2++4H+=2Fe3++Mn 2++2H2O,物质X可以是BD(用字母表示.
A.Cu2(OH)2CO3 B.MnCO3 C.MgO D.Zn(OH)2
(4)流程中可以循环利用的物质是H2SO4(填化学式).
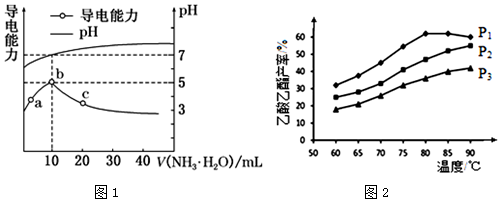
(5)MnO2与Li构成LiMnO2,该电池反应原理如图2所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
①外电路中的电子移动方向是由a极流向b极(填字母).
②写出该锂离子电池的正极电极反应式MnMnO2+e-+Li+=LiMnO2.
(6)已知:25℃时,HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,该反应的化学方程式为NaCN+H2S=HCN+NaHS.

已知:I.矿石中所有金属元素在滤液中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式3MnO2+2FeS+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$3MnSO4+Fe2(SO4)3+2S+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③与MnO2发生氧化还原反应的离子方程式MnO2+2Fe2++4H+=2Fe3++Mn 2++2H2O,物质X可以是BD(用字母表示.
A.Cu2(OH)2CO3 B.MnCO3 C.MgO D.Zn(OH)2
(4)流程中可以循环利用的物质是H2SO4(填化学式).
(5)MnO2与Li构成LiMnO2,该电池反应原理如图2所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
①外电路中的电子移动方向是由a极流向b极(填字母).
②写出该锂离子电池的正极电极反应式MnMnO2+e-+Li+=LiMnO2.
(6)已知:25℃时,HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,该反应的化学方程式为NaCN+H2S=HCN+NaHS.
17.NA为阿伏加德罗常数的值.下列说法正确是( )
| A. | 44g CO2和N2O的混合物中含有的氧原子数为1.5NA | |
| B. | 2L 0.5mol/L亚硫酸氢钠溶液中含有的HSO3-离子数为NA | |
| C. | 0.5mol CH5+中含有的电子数目为5NA | |
| D. | 常温下,1L 0.5 mol/L Ba(OH)2溶液中水电离的OH-个数为0.1NA |
16.有关HF和HCl判断正确的是( )
| A. | 键长:HF>HCl | B. | 键能:HF>HCl | ||
| C. | 稳定性:HCl>HF | D. | 共用电子对偏移程度:HCl>HF |
15.既能和盐酸反应,又能和氢氧化钠溶液反应的物质是( )
| A. | Fe | B. | Fe2O3 | C. | Al | D. | AlCl3 |
14.将两种互不相溶的液体分离的方法是( )
| A. | 分液 | B. | 结晶 | C. | 纸层析 | D. | 过滤 |
13.对于可逆反应2A(g)+3B(g)?3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是( )
0 162746 162754 162760 162764 162770 162772 162776 162782 162784 162790 162796 162800 162802 162806 162812 162814 162820 162824 162826 162830 162832 162836 162838 162840 162841 162842 162844 162845 162846 162848 162850 162854 162856 162860 162862 162866 162872 162874 162880 162884 162886 162890 162896 162902 162904 162910 162914 162916 162922 162926 162932 162940 203614
| A. | 各物质的量浓度之比为c(A):c(B):c(C)=2:3:3 | |
| B. | 正逆反应速率相等且等于零 | |
| C. | 平衡混合物中各物质的量浓度相等 | |
| D. | 单位时间内,若消耗了amolA物质,则同时也消耗了1.5amolC物质 |