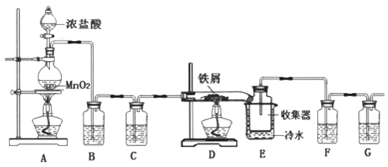
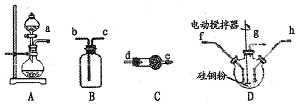
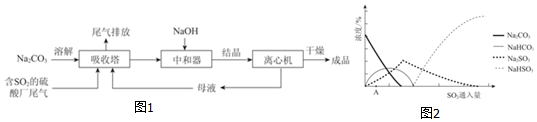
4.已知HF 酸性强于CH3COOH,常温下有下列三种溶液.有关叙述不正确的是( )
| 编号 | ① | ② | ③ |
| PH | 11 | 3 | 3 |
| 溶液 | NaOH溶液 | CH3COOH溶液 | HF溶液 |
| A. | CH3COOH稀溶液中加入少量CH3COONa,能使比值c(CH3COO-)/c(Na+)增大 | |
| B. | ①、②等体积很合后:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 向②加入NaF固体,CH3COOH电离平衡正向移动 | |
| D. | 中和相同体积的②、③,需消耗①的体积②<③ |
2.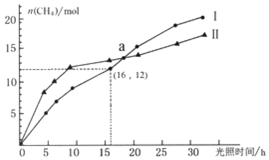 可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g)?CH4(g)+2O2(g)△H=+802KJ/mol,右图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线.下列说法正确的是( )
可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g)?CH4(g)+2O2(g)△H=+802KJ/mol,右图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线.下列说法正确的是( )
 可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g)?CH4(g)+2O2(g)△H=+802KJ/mol,右图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线.下列说法正确的是( )
可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g)?CH4(g)+2O2(g)△H=+802KJ/mol,右图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线.下列说法正确的是( )| A. | 0-15h内,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好 | |
| B. | 反应开始后的30h内,第Ⅰ种催化剂的作用下,反应吸收的热量多 | |
| C. | a点时,CO2的转化率相等 | |
| D. | 0-16h内,v(O2)=1.5mol/(L•h) |
1.下列说法不正确的是( )
| A. | 化学键的断裂与形成一定伴随着电子的转移和能量变化 | |
| B. | 碘晶体是分子晶体,加热升华过程中只需克服分子间作用力 | |
| C. | 二氧化硅晶体属于原子晶体,每个Si通过共价键与4个O结合 | |
| D. | 氯化钠的电离是一个破坏离子键的过程 |
20.为探究铝片与不同浓度氯化铜溶液的反应,某学习小组将打磨好的同样大小的小块铝片放入3mL不同浓度CuCl2溶液中进行了如表实验:
(1)①推测红色固体是铜,写出生成铜反应的离子方程式2Al+3 Cu2+=2Al3++3Cu
②部分同学提出假设,认为红色固体中可能含有红色的氧化亚铜,查阅资料:
i. 氧化亚铜能溶于氯化铁溶液生成铜盐.
ii.氧化亚铜能溶于浓氨水形成无色配合物[Cu(NH3)2]+,其在空气中易被氧化成蓝色的[Cu(NH3)4(H2O)2]2+.
进行如下实验:将实验I所得溶液过滤,洗涤,加入浓氨水震荡,静置一段时间后溶液未变蓝色,证明红色固体中不含氧化亚铜.
(2)推测气体是氢气,写出氯化铜溶液显酸性的离子方程式:Cu2++2H2O=Cu(OH)2+2 H+.
试从以下角度分析开始一段时间内产生气体的速率不断加快的原因:
①浓度:随着反应的进行c(Al3+)增大,水解产生的c(H+)增大,产生氢气的速率加快.
②能量:因反应放热,温度升高,产生氢气的速率加快.
③电化学:铝与置换出的铜构成铝铜原电池,产生氢气的速率加快.
(3)探究白色沉淀的成分:
取实验ii所得混合液过滤,洗涤.将所得固体分成两份,一份加入浓盐酸,震荡白色沉淀消失:另一份加入浓氨水溶液,白色沉淀消失.
资料1:CuCl为白色固体,难溶于水,溶于浓盐酸,溶于浓氨水成无色溶液;CuCl与氢氧化钠反应转化为CuOH为橙黄色沉淀.
资料2:制备CuCl的方法有二
i.Cu和CuCl2在浓盐酸中反应,将得到的溶液稀释后生成CuCl
ii.Cu和CuCl2溶液加热即可得到CuCl
①推测白色沉淀中不含Al(OH)3,判断依据是加入浓氨水,白色沉淀不消失含有Al(OH)3,反之不含,因 Al(OH)3是两性氢氧化物,但不溶于弱碱氨水.
②推测白色沉淀是CuCl,探究白色沉淀的形成过程.设计实验:取3mL,2.00mol/LCuCl2溶液加入少量Cu粉并加热证明该白色沉淀的生成与铝和氯化铝无关.
③在白色沉淀中加入氢氧化钠溶液,产生橙黄色沉淀,从平衡移动角度进行解释:CuCl在水溶液中存在溶解平衡CuCl(S)?Cu+(aq)+Cl-(aq),加入氢氧化钠溶液,Cu+与反应生成橙黄色的CuOH沉淀,使溶解平衡正向移动,实现沉淀转化.
| 实验 | c(CuCl2) | 实验现象 |
| I | 0.25mol/L | 有红色固体析出,有气泡冒出,一段时间内出气速率加快. |
| II | 2.00mol/L | 反应剧烈,有红色固体析出,产生大量气泡,有白色难溶物,试管外壁温度明显升高,一段时间内出气速率加快. |
②部分同学提出假设,认为红色固体中可能含有红色的氧化亚铜,查阅资料:
i. 氧化亚铜能溶于氯化铁溶液生成铜盐.
ii.氧化亚铜能溶于浓氨水形成无色配合物[Cu(NH3)2]+,其在空气中易被氧化成蓝色的[Cu(NH3)4(H2O)2]2+.
进行如下实验:将实验I所得溶液过滤,洗涤,加入浓氨水震荡,静置一段时间后溶液未变蓝色,证明红色固体中不含氧化亚铜.
(2)推测气体是氢气,写出氯化铜溶液显酸性的离子方程式:Cu2++2H2O=Cu(OH)2+2 H+.
试从以下角度分析开始一段时间内产生气体的速率不断加快的原因:
①浓度:随着反应的进行c(Al3+)增大,水解产生的c(H+)增大,产生氢气的速率加快.
②能量:因反应放热,温度升高,产生氢气的速率加快.
③电化学:铝与置换出的铜构成铝铜原电池,产生氢气的速率加快.
(3)探究白色沉淀的成分:
取实验ii所得混合液过滤,洗涤.将所得固体分成两份,一份加入浓盐酸,震荡白色沉淀消失:另一份加入浓氨水溶液,白色沉淀消失.
资料1:CuCl为白色固体,难溶于水,溶于浓盐酸,溶于浓氨水成无色溶液;CuCl与氢氧化钠反应转化为CuOH为橙黄色沉淀.
资料2:制备CuCl的方法有二
i.Cu和CuCl2在浓盐酸中反应,将得到的溶液稀释后生成CuCl
ii.Cu和CuCl2溶液加热即可得到CuCl
①推测白色沉淀中不含Al(OH)3,判断依据是加入浓氨水,白色沉淀不消失含有Al(OH)3,反之不含,因 Al(OH)3是两性氢氧化物,但不溶于弱碱氨水.
②推测白色沉淀是CuCl,探究白色沉淀的形成过程.设计实验:取3mL,2.00mol/LCuCl2溶液加入少量Cu粉并加热证明该白色沉淀的生成与铝和氯化铝无关.
③在白色沉淀中加入氢氧化钠溶液,产生橙黄色沉淀,从平衡移动角度进行解释:CuCl在水溶液中存在溶解平衡CuCl(S)?Cu+(aq)+Cl-(aq),加入氢氧化钠溶液,Cu+与反应生成橙黄色的CuOH沉淀,使溶解平衡正向移动,实现沉淀转化.
19.研究碳、氮及其化合物的转化对于环境的改善有重大意义.
(1)氧化还原法消除NOx的转化如下:NO$→_{反应Ⅰ}^{O_{3}}$NO2$→_{反应Ⅱ}^{CO(NH_{2})_{2}}$N2
已知:NO(g)+O3(g)═NO2(g)+O2(g)△H=-200.9kJ/mol
2NO(g)+O2(g)═2NO(g)△H=-116.2kJ/mol
则反应I的热化学方程式为3NO(g)+O3(g)═3NO2(g)△H=-317.1 kJ•mol-1.
(2)有人设想将CO按下列反应除去:2CO(g)═2C(s)+O2(g)△H>0,请你分析该设想能否实现?否(填“是”或“否”),依据是该反应是焓增、熵减的反应,根据G=△H-T•△S,G>0.
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠.已知常温时,甲酸的电离平衡常数Ka=1.70×10-4.
①甲酸钠的水溶液呈碱性,请用离子反应方程式表示其原因HCOO-+H2O?HCOOH+OH-.
②向20mL 0.1mol/L的甲酸钠溶液中滴加10ml 0.1mol/L的盐酸,混合液呈酸性(填“酸”或“碱”),溶液中离子浓度从大到小的顺序为c(Na+)>c(HCOO-)>c(Cl-)>c(H+)>c(OH-).
(4)活性炭也可用于处理汽车尾气中的NO.在2L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如表:
①该反应的正反应为放热(填”吸热”或“放热”)反应.
②200℃时,平衡后向恒容容器中再充入0.1molNO,再次平衡后,NO的百分含量将不变.(填“增大”、“减小”或“不变”).
③计算反应体系在335℃时的平衡常数0.25.
0 161527 161535 161541 161545 161551 161553 161557 161563 161565 161571 161577 161581 161583 161587 161593 161595 161601 161605 161607 161611 161613 161617 161619 161621 161622 161623 161625 161626 161627 161629 161631 161635 161637 161641 161643 161647 161653 161655 161661 161665 161667 161671 161677 161683 161685 161691 161695 161697 161703 161707 161713 161721 203614
(1)氧化还原法消除NOx的转化如下:NO$→_{反应Ⅰ}^{O_{3}}$NO2$→_{反应Ⅱ}^{CO(NH_{2})_{2}}$N2
已知:NO(g)+O3(g)═NO2(g)+O2(g)△H=-200.9kJ/mol
2NO(g)+O2(g)═2NO(g)△H=-116.2kJ/mol
则反应I的热化学方程式为3NO(g)+O3(g)═3NO2(g)△H=-317.1 kJ•mol-1.
(2)有人设想将CO按下列反应除去:2CO(g)═2C(s)+O2(g)△H>0,请你分析该设想能否实现?否(填“是”或“否”),依据是该反应是焓增、熵减的反应,根据G=△H-T•△S,G>0.
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠.已知常温时,甲酸的电离平衡常数Ka=1.70×10-4.
①甲酸钠的水溶液呈碱性,请用离子反应方程式表示其原因HCOO-+H2O?HCOOH+OH-.
②向20mL 0.1mol/L的甲酸钠溶液中滴加10ml 0.1mol/L的盐酸,混合液呈酸性(填“酸”或“碱”),溶液中离子浓度从大到小的顺序为c(Na+)>c(HCOO-)>c(Cl-)>c(H+)>c(OH-).
(4)活性炭也可用于处理汽车尾气中的NO.在2L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如表:
| 固体活性炭/mol | NO/mol | A/mol | B/mol | |
| 200℃ | 2.000 | 0.0400 | 0.0300 | 0.0300 |
| 335℃ | 2.005 | 0.0500 | 0.0250 | 0.0250 |
②200℃时,平衡后向恒容容器中再充入0.1molNO,再次平衡后,NO的百分含量将不变.(填“增大”、“减小”或“不变”).
③计算反应体系在335℃时的平衡常数0.25.

 、K
、K .
. .(本题不考虑
.(本题不考虑 结构).
结构).