4.用CO2、CO合成甲醇是碳减排的新方向,其发生的化学方程式如下:CO2+3H2?CH3OH+H2O;CO+2H2?CH3OH,若CO2和CO混合气共消耗H2 10mol,生成甲醇4mol,则参加反应的CO2是( )
| A. | 1 mol | B. | 2 mol | C. | 3 mol | D. | 4 mol |
3.以下实验操作方法正确的是( )
| A. | 除去Cl2中的HCl:将混合气体通过AgNO3溶液 | |
| B. | 除去C2H6中的C2H4:将混合气体通过酸性KMnO4溶液 | |
| C. | 检验CO2中是否混有HCl:将气体通入饱和NaHCO3溶液 | |
| D. | 检验Cl2中是否混有空气:将装有气体的试管倒置在NaOH溶液中 |
2.等体积等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合,离子方程式正确的是( )
| A. | CO32-+Ba2+→BaCO3↓ | |
| B. | HCO3-+OH-→H2O+CO32- | |
| C. | HCO3-+Ba2++OH-=H2O+BaCO3↓ | |
| D. | 2HCO3-+Ba2++2OH-→BaCO3↓+2H2O+CO32- |
1.用饱和氯化钠溶液润湿的滤纸分别做甲、乙两个实验,下列判断错误的是( )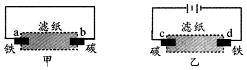

| A. | 甲是原电池,乙是电解池 | |
| B. | 甲中铁棒比乙中铁棒更易腐蚀 | |
| C. | d电极上的电极反应是:Fe-2e→Fe2+ | |
| D. | b电极上的电极反应是:O2+2H2O+4e→4OH- |
20.以下物质的制备用错实验装置的是( )
| A. | 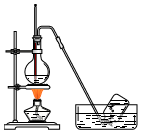 乙烯的制取 | B. |  乙酸乙酯的制备 | C. |  乙酸丁酯的制备 | D. |  乙炔的制取 |
19.下列工业生产的条件选择与勒沙特列原理无关的是( )
| A. | 工业合成氯化氢时使用过量氢气 | |
| B. | 硫酸工业接触室中使用过量空气 | |
| C. | 合成氨工业采用20~50 MPa高压 | |
| D. | 侯氏制碱法向母液中加入氯化钠提取氯化铵 |
18.某反应A(g)+B(g)?C(g)的能量变化如图所示,由图象可知,加入X后( )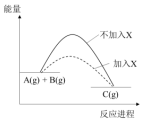

| A. | 反应速率增大 | B. | 反应物转化率增大 | ||
| C. | 生成物的能量降低 | D. | 反应的热效应降低 |
17.0.1mol/L Na2S溶液中,微粒间关系正确的是( )
| A. | [Na+]+[H+]=[OH-]+[HS-]+[S2-] | B. | [Na+]>[S2-]>[HS-]>[OH-] | ||
| C. | [Na+]=2[S2-]+2[HS-]+2[H2S] | D. | [Na+]>[HS-]>[S2-]>[OH-] |
16.由水电离出来的氢离子浓度为10-13 mol/L,在此溶液中一定能大量共存的离子组是( )
0 160669 160677 160683 160687 160693 160695 160699 160705 160707 160713 160719 160723 160725 160729 160735 160737 160743 160747 160749 160753 160755 160759 160761 160763 160764 160765 160767 160768 160769 160771 160773 160777 160779 160783 160785 160789 160795 160797 160803 160807 160809 160813 160819 160825 160827 160833 160837 160839 160845 160849 160855 160863 203614
| A. | ClO-、K+、Cl- | B. | Ba2+、Na+、Br- | C. | Na+、Fe3+、SO42- | D. | K+、NO3-、NH4+ |
 ,其属于非极性(填“极
,其属于非极性(填“极