11.下列实验操作不正确或不能达到目的是( )
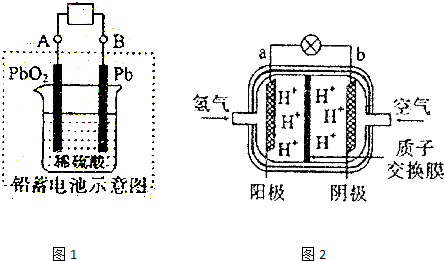
| A. | 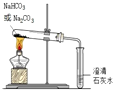 鉴别碳酸钠和碳酸氢钠 | |
| B. | 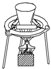 钠的燃烧 | |
| C. | 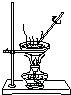 直接蒸发氯化铁溶液获得氯化铁晶体 | |
| D. | 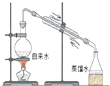 实验室制取蒸馏水 |
10.四种短周期元素X、Y、Z、W的原子序数依次增大.X与Z位于同一主族,Y元素的单质既能与盐酸反应又能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14.下列说法正确的是( )
| A. | Y的阳离子半径比W的阴离子半径小 | |
| B. | 气态氢化物的稳定性:X<Z<W | |
| C. | X、Z、W的氧化物对应的水化物的酸性强弱:X<Z<W | |
| D. | 室温下,含Y元素的盐形成的水溶液的pH<7 |
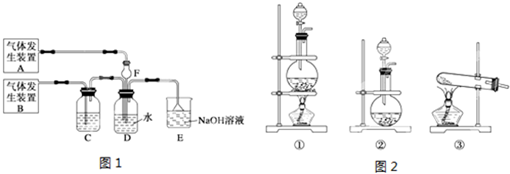
8.为研究某铁钉与浓硫酸反应生成气体Y的成分,某学习小组做出假设,认为所得气体中除含有SO2外,还可能含有H2和Q气体,并设计了下列实验装置(图中夹持仪器省略)探究气体的成分,为确认Q的存在,需在装置中添加M于( )


| A. | A-B之前 | B. | B-C间 | C. | C-D间 | D. | D-E间 |
7.下列离子方程式书写正确的是( )
| A. | 向次氯酸钙溶液通过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+CO32-+H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+5I-+6H+=3I2+3H2O | |
| D. | 氢氧化钡溶液中加入硫酸:Ba2++OH-+H++SO42-═BaSO4+H2O |
6.从下列事实所列出的相应结论正确的是( )
| 实 验 事 实 | 结 论 | |
| ① | SO2使酸性高锰酸钾溶液褪色 | 可证明SO2有漂白性 |
| ② | 浓盐酸可除去烧瓶内残留的MnO2,稀硝酸可除去试管内壁的银镜,用磨口玻璃瓶保存NaOH溶液 | 都发生了氧化还原反应 |
| ③ | 取少量Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀滴加稀盐酸,沉淀不溶解, | 证明Na2SO3已氧化变质 |
| ④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
| ⑤ | 某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A. | ②⑤ | B. | ①② | C. | ④⑤ | D. | 全部 |
5.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 由2H和18O所组成的水22g,其中所含的中子数为11 NA | |
| B. | 分子数为NA的N2、CO混合气体体积为22.4 L,质量为28 g | |
| C. | 标准状况下,22.4LNO和11.2L O2混合后气体的原子总数为3NA | |
| D. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA |
4.下列现象或事实不能用同一原理解释的是( )
| A. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| B. | 硫化钠和硫酸亚铁固体长期暴露在空气中变质 | |
| C. | 常温下铁和铂都不溶于浓硝酸 | |
| D. | H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率 |
3.下列表述正确的是( )
①某物质经科学测定只含有一种元素,不可以断定该物质一定是一种纯净物;
②过量铁粉在氯气中燃烧生成FeCl2
③浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸;
④医疗上用的“钡餐”其成分是碳酸钡,漂白粉的成分为次氯酸钙;
⑤高压钠灯发出的黄光射程远,透雾能力强,故可做航标灯
⑥能与酸反应的氧化物,一定是碱性氧化物.
0 159476 159484 159490 159494 159500 159502 159506 159512 159514 159520 159526 159530 159532 159536 159542 159544 159550 159554 159556 159560 159562 159566 159568 159570 159571 159572 159574 159575 159576 159578 159580 159584 159586 159590 159592 159596 159602 159604 159610 159614 159616 159620 159626 159632 159634 159640 159644 159646 159652 159656 159662 159670 203614
①某物质经科学测定只含有一种元素,不可以断定该物质一定是一种纯净物;
②过量铁粉在氯气中燃烧生成FeCl2
③浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸;
④医疗上用的“钡餐”其成分是碳酸钡,漂白粉的成分为次氯酸钙;
⑤高压钠灯发出的黄光射程远,透雾能力强,故可做航标灯
⑥能与酸反应的氧化物,一定是碱性氧化物.
| A. | ①②③ | B. | ①③⑤ | C. | ②④⑥ | D. | ②③⑤ |