15.下列行为中符合安全要求的是( )
| A. | 进入煤矿矿井时,用火把照明 | |
| B. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| C. | 实验时,蒸发结晶时,当有大量晶体析出时再用玻璃棒搅拌 | |
| D. | 装运乙醇的包装箱上应贴上易燃液体的危险品标志图标 |
14.下列说法中正确的是( )
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化都是化学变化 | |
| C. | 在吸热反应中,反应物的总能量高于生成物的总能量 | |
| D. | 需要加热的化学反应一定是放热反应 |
12.表是有机物A、B的有关信息.
根据表中信息回答下列问题:
(1)A的名称是:乙烯
(2)写出在一定条件下,A生成高分子化合物的化学反应方程式 .
.
(3)B的名称为:苯.B与乙苯互为同系物.其中乙苯的同分异构体还3 种.写出其中一种的物质名称邻二甲苯(或间二甲苯或对二甲苯).
| A | B |
| ②使溴的四氯化碳溶液褪色; ②比例模型为: 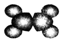 ③能与水在一定条件下反应生成醇 | ①由C、H两种元素组成; ②球棍模型为: 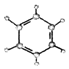 |
(1)A的名称是:乙烯
(2)写出在一定条件下,A生成高分子化合物的化学反应方程式
 .
.(3)B的名称为:苯.B与乙苯互为同系物.其中乙苯的同分异构体还3 种.写出其中一种的物质名称邻二甲苯(或间二甲苯或对二甲苯).
9.常温下,下列有关溶液的说法不正确的是( )
| A. | Na2CO3、NaHCO3两种盐溶液中,离子种类相同 | |
| B. | 物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者 | |
| C. | 某物质的水溶液中由水电离出的c(H+)=1×10-amol/L,若a>7,则该溶液的pH为a或14-a | |
| D. | 相同温度下,0.2mol/L的醋酸溶液与0.1mol/L的醋酸溶液中c(H+)之比大于2:1 |
8.在下列各组的比较中,前者比后者大的是( )
| A. | 同温度、同浓度的NaCl溶液和氨水的导电能力 | |
| B. | 25℃时.pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度 | |
| C. | 25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度 | |
| D. | 25℃时.pH均为3的盐酸和FeCI3溶液中水的电离程度 |
7.科学家正在研究利用催化技术将汽车尾气中的NO和CO转变成CO2和N2化学方程式如下:2NO(g)+2CO(g) $\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g)△H.
为了测定在某种催化剂作用下的反应速度,某温度下,在容积固体的容器内进行此反应,并用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在该反应的平衡常数的表达式K=$\frac{{{c^2}(C{O_2})•c({N_2})}}{{{c^2}(NO)•{c^2}(CO)}}$.
(2)该反应在此温度下能够自发进行,说明△H<0(填写“>”、“<”、“=”).
若只将反应条件改为绝热,平衡时NO的浓度将增大(填“增大”、“减小”、“不变”)
(3)前2s内的平均反应速率v(N21.88×10-4mol•L-1•s-1.
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
(5)请在上表空格中填入剩余的实验条件数据.
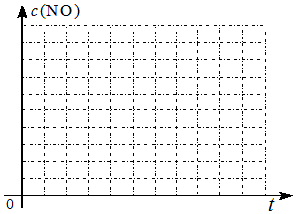
(6)请在给出的坐标图中,参考实验 I实验条件下混合气体中NO浓度随时间变化的趋势曲线图,画出 II、III条曲线图,并标明各条曲线的实验编号.
0 159431 159439 159445 159449 159455 159457 159461 159467 159469 159475 159481 159485 159487 159491 159497 159499 159505 159509 159511 159515 159517 159521 159523 159525 159526 159527 159529 159530 159531 159533 159535 159539 159541 159545 159547 159551 159557 159559 159565 159569 159571 159575 159581 159587 159589 159595 159599 159601 159607 159611 159617 159625 203614
为了测定在某种催化剂作用下的反应速度,某温度下,在容积固体的容器内进行此反应,并用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)在该反应的平衡常数的表达式K=$\frac{{{c^2}(C{O_2})•c({N_2})}}{{{c^2}(NO)•{c^2}(CO)}}$.
(2)该反应在此温度下能够自发进行,说明△H<0(填写“>”、“<”、“=”).
若只将反应条件改为绝热,平衡时NO的浓度将增大(填“增大”、“减小”、“不变”)
(3)前2s内的平均反应速率v(N21.88×10-4mol•L-1•s-1.
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
| 实验编号 | T(℃) | NO初始浓度 (mol/L) | C O初始浓度 (mol/L) | 催化剂的比表面积 (m2/g) |
| 1 | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| 2 | 124 | |||
| 3 | 350 | 124 |
(6)请在给出的坐标图中,参考实验 I实验条件下混合气体中NO浓度随时间变化的趋势曲线图,画出 II、III条曲线图,并标明各条曲线的实验编号.
