11.下列关于胶体的叙述正确的是( )
| A. | 胶体是很稳定的分散系,比溶液还稳定 | |
| B. | 胶体能发生丁达尔现象 | |
| C. | 胶体的分散质不能透过滤纸 | |
| D. | 胶体不稳定,静止后容易产生沉淀 |
10.胶体区别于其他分散系的本质特征是( )
| A. | 胶体是澄清透明的 | B. | 胶体能产生丁达尔现象 | ||
| C. | 分散质粒子直径在1nm~100nm之间 | D. | 胶体在一定条件下能稳定存在 |
5.如图是a、b两种固体物质(不含结晶水)的溶解度曲线.下列说法正确的是( )
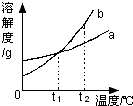

| A. | b的溶解度大于a的溶解度 | |
| B. | t1℃时,将a、b两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等 | |
| C. | 将t2℃时的b的不饱和溶液降温至t1℃,一定能得到b的饱和溶液 | |
| D. | t2℃时,a溶液的溶质质量分数一定小于b溶液的溶质质量分数 |
3.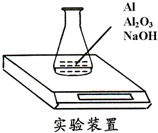 某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:
某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:
(1)反应中产生的氢气质量为0.06g.
(2)求样品中Al的质量分数.(要求有计算过程)
 某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:
某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:| 读数次数 | 质量(g) | |
| 锥形瓶 + NaOH溶液 + 试样 | 第1次 | 188.30 |
| 第2次 | 188.28 | |
| 第3次 | 188.25 | |
| 第4次 | 188.24 | |
| 第5次 | 188.24 |
(2)求样品中Al的质量分数.(要求有计算过程)
2.钠投入滴有酚酞的水中,不能证明钠具有下列哪些性质?( )
0 158147 158155 158161 158165 158171 158173 158177 158183 158185 158191 158197 158201 158203 158207 158213 158215 158221 158225 158227 158231 158233 158237 158239 158241 158242 158243 158245 158246 158247 158249 158251 158255 158257 158261 158263 158267 158273 158275 158281 158285 158287 158291 158297 158303 158305 158311 158315 158317 158323 158327 158333 158341 203614
| A. | 钠的密度比水小 | B. | 钠的熔点低 | ||
| C. | 钠与水反应放出气体 | D. | 钠与水反应有酸生成 |




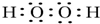 .W、X、Y 的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)
.W、X、Y 的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)
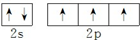 .
.