14.下列关于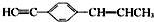 的说法正确的是( )
的说法正确的是( )
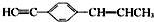 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子有可能都在同一个平面上 | |
| B. | 最多可能有9个碳原子在同一平面上 | |
| C. | 只能有4个碳原子在同一直线上 | |
| D. | 有7个碳原子可能在同一条直线上 |
13.有两种有机物Q( )与P(
)与P( ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )
 )与P(
)与P( ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )| A. | 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3:1 | |
| B. | 二者在NaOH醇溶液中均可发生消去反应 | |
| C. | 一定条件下,二者在NaOH溶液中均可发生取代反应 | |
| D. | Q的一氯代物只有1种,P的一溴代物有2种 |
12.下列有机物的命名正确的是( )
| A. | 4,4,3-三甲基己烷 | B. | 2-甲基-4-乙基戊烷 | ||
| C. | 3-甲基-2-戊炔 | D. | 2,2-二甲基戊烷 |
9.下列粒子的半径关系正确的是( )
| A. | r(Na)>r(Mg)>r(Al)>r(K) | B. | r(K+)>r(Ca2+)>r(S2-)>r(Cl-) | ||
| C. | r(Na)>r(K)>r(Ca)>r(Mg) | D. | r(F-)>r(Na+)>r(Mg2+)>r(Al3+) |
8.下列原子结构示意图中,正确的是( )
| A. | 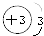 | B. |  | C. | 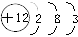 | D. | 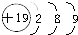 |
6.对烷烃CH3CH(C2H5)CH(C2H5)CH(CH3)2的命名,正确的是( )
0 154629 154637 154643 154647 154653 154655 154659 154665 154667 154673 154679 154683 154685 154689 154695 154697 154703 154707 154709 154713 154715 154719 154721 154723 154724 154725 154727 154728 154729 154731 154733 154737 154739 154743 154745 154749 154755 154757 154763 154767 154769 154773 154779 154785 154787 154793 154797 154799 154805 154809 154815 154823 203614
| A. | 2,3-二甲基-4-乙基戊烷 | B. | 2-甲基3,4-二乙基戊烷 | ||
| C. | 2,4-二甲基-3-乙基己烷 | D. | 2,5-二甲基-3-乙基己烷 |
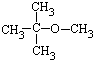 .
.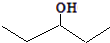 ,乙所含官能团的名称为羟基.
,乙所含官能团的名称为羟基. .
.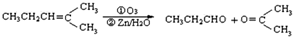
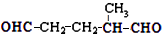 ,则烃A的结构可表示为
,则烃A的结构可表示为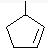 .
.

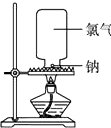 下面是钠和氯气反应的实验设计:
下面是钠和氯气反应的实验设计: