题目内容
10.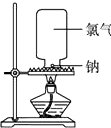 下面是钠和氯气反应的实验设计:
下面是钠和氯气反应的实验设计:(1)实验步骤:取一块绿豆大的金属钠(切去氧化层),用滤纸吸净煤油,放在石棉网上,用酒精灯微热.待钠熔成球状时,将盛有氯气的集气瓶迅速倒扣在钠的上方,观察现象.
(2)记录实验现象
| 现象 | |
| 化学方程式 |
分析 钠的熔点低,首先熔化成闪亮的小球,然后剧烈燃烧,产生大量白烟,由此分析解答.
解答 解:钠的熔点低,首先熔化成闪亮的小球,然后剧烈燃烧生成氯化钠固体小颗粒,所以观察到产生大量白烟,反应的化学方程式为2Na+Cl2═2NaCl,
故答案为:钠首先熔化成闪亮的小球,然后剧烈燃烧,产生大量白烟;2Na+Cl2═2NaCl.
点评 本题考查氯气与钠反应的实验设计,题目难度中等,学习中牢固掌握相关基础知识,把握相关实验操作,则本题不易出错.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强.25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)?Cl2(aq) K1=10-1.2
Cl2(aq)+H2O?HClO+H++Cl- K2=10-3.4
HClO?H++ClO- Ka=?
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示.下列表述正确的是( )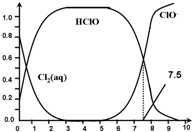
Cl2(g)?Cl2(aq) K1=10-1.2
Cl2(aq)+H2O?HClO+H++Cl- K2=10-3.4
HClO?H++ClO- Ka=?
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示.下列表述正确的是( )

| A. | Cl2(g)+H2O?2H++ClO-+Cl- K=10-12.1 | |
| B. | 在氯处理水体系中,c(HClO)+c(ClO-)=c(H+)-c(OH-) | |
| C. | 用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时好 | |
| D. | 氯处理饮用水时,在夏季的杀菌效果比在冬季好 |
4.X、Y、Z均为短周期主族元素,X为地壳中含量最高的金属元素,Y的L层电子数等于K层电子数的3倍,Z元素M层电子数为7,下列有关说法不正确的是( )
| A. | X与Y形成的化合物既能与盐酸反应也能与氢氧化钠反应 | |
| B. | X的原子半径大于Z的原子半径 | |
| C. | X与Z形成的化合物的水溶液中逐滴滴加氨水至过量,先产生白色沉淀后沉淀溶解 | |
| D. | Z的最高价氧化物对应的水化物为强酸 |
5.下列物质中,既有离子键,又有非极性共价键的是( )
| A. | H2O | B. | CaCl2 | C. | KOH | D. | Na2O2 |

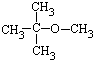 .
.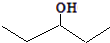 ,乙所含官能团的名称为羟基.
,乙所含官能团的名称为羟基. .
.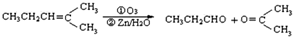
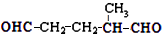 ,则烃A的结构可表示为
,则烃A的结构可表示为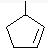 .
. .
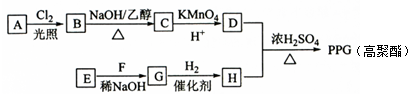
.

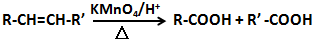
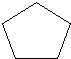 .
.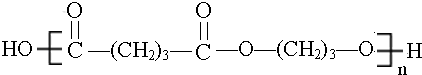 .
. ;
; .
.