20.电离常数(Ka或Kb)、水解平衡常数(Kh)、溶度积常数(Ksp)是判断物质性质的重要常数,下列关于这些常数的计算或运用正确的是( )
| A. | 某温度下,0.1mol•L-1的醋酸溶液PH=3,则其电离常数Ka≈1.0×10-4 | |
| B. | Ka、Kb、Kh均随温度升高而增大 | |
| C. | 弱酸HA的电离平衡常数为Ka,则A-的水解平衡常数为Kh=Ka•Kw | |
| D. | 因为Ksp(AgCl)<Ksp(AgOH),所以AgCl不溶于稀硝酸 |
19.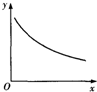 在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
 在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )| 选项 | x | y |
| A | 温度 | 混合气体平均相对分子质量 |
| B | 压强 | S2气体体积分数 |
| C | 容器体积 | H2S浓度 |
| D | O2浓度 | 平衡常数 |
| A. | A | B. | B | C. | C | D. | D |
18.配置一定物质的量浓度的硫酸溶液是,下列操作会造成所配硫酸溶液浓度偏低的是( )
| A. | 洗涤了量取浓硫酸的量筒,并把洗涤液转移到容量瓶中 | |
| B. | 转移溶液前,容量瓶中含有少量蒸馏水 | |
| C. | 溶解硫酸用的烧杯、玻璃棒未洗涤 | |
| D. | 定容时俯视容量瓶的刻度线 |
16.使用酸碱中和滴定的方法,用0.01mol/L盐酸滴定锥形瓶中未知浓度的NaOH溶液,下列操作能够使测定结果偏高的是( )
| A. | 用量筒量取浓盐酸配制0.01mol/L稀盐酸时,量筒用蒸馏水洗净后未经干燥直接量取浓盐酸 | |
| B. | 配制稀盐酸定容时,俯视容量瓶刻度线 | |
| C. | 滴定前尖嘴处无气泡,滴定终点时有气泡 | |
| D. | 滴定过程中用少量蒸馏水将锥形瓶内避粘附的盐酸冲下 |
15.下列由实验现象得出的结论正确的是( )
| A. | 向某无色液中加BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有Ag+ | |
| B. | 向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32- | |
| C. | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,说明NH4Cl固体可以升华 | |
| D. | 向NaBr溶液中滴入少量氯水和CCl4,振荡、静置,溶液下层呈橙红色,说明Br-还原性强于Cl- |
13.(1)已知有机物之间转化关系如下:(部分条件省略)
A(C4H8)$\stackrel{溴水}{→}$ B(C4H8Br2)→C(C4H6)$\stackrel{溴水}{→}$
①A物质的结构简式CH3CH=CHCH3
②C物质的名称1,3-丁二烯
③B→C的化学方程式 +2NaOH$→_{△}^{乙醇}$CH2=CHCH=CH2↑+2NaBr+2H2O
+2NaOH$→_{△}^{乙醇}$CH2=CHCH=CH2↑+2NaBr+2H2O
(2)芳香族化合物A、B、C的分子式均为C7H8O
①A、B、C互为同分异构体
②A、B、C的结构简式分别为
A B
B C
C
③A与浓溴水反应的方程式
④A的钠盐溶液中通入CO2的方程式
⑤B与金属钠反应的方程式 .
.
A(C4H8)$\stackrel{溴水}{→}$ B(C4H8Br2)→C(C4H6)$\stackrel{溴水}{→}$

①A物质的结构简式CH3CH=CHCH3
②C物质的名称1,3-丁二烯
③B→C的化学方程式
 +2NaOH$→_{△}^{乙醇}$CH2=CHCH=CH2↑+2NaBr+2H2O
+2NaOH$→_{△}^{乙醇}$CH2=CHCH=CH2↑+2NaBr+2H2O(2)芳香族化合物A、B、C的分子式均为C7H8O
| A | B | C | |
| 加入氯化铁溶液 | 显紫色 | 无明显现象 | 无明显现象 |
| 加入钠 | 放出氢气 | 放出氢气 | 不反应 |
| 苯环上一氯代物的种数 | 2 | 3 | 3 |
②A、B、C的结构简式分别为
A
 B
B C
C
③A与浓溴水反应的方程式

④A的钠盐溶液中通入CO2的方程式

⑤B与金属钠反应的方程式
 .
.
12.某学习小组共同学习乙醛的化学性质,以下是他们的学习过程,请填空:
(1)根据乙醛的结构对性质进行预测
(2)写出乙醛与氢气反应的方程式CH3CHO+H2$→_{△}^{催化剂}$CH3CH2OH
(3)设计实验验证乙醛的还原性,请填全表格.
根据上表及所学知识回答:
①乙醛被高锰酸钾溶液氧化为CH3COOH(填结构简式)
②写出乙醛发生银镜反应的方程式CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O
(4)某有机物只含C、H、O三种元素,该有机物对氢气的相对密度为15,完全燃烧 0.1mol该有机物生成4.4gCO2和1.8gH2O,该有机物的分子式为CH2O,若红外光谱显示该分子中有醛基,则3g该物质与足量的新制氢氧化铜反应,生成沉淀的质量为28.8g.
0 153675 153683 153689 153693 153699 153701 153705 153711 153713 153719 153725 153729 153731 153735 153741 153743 153749 153753 153755 153759 153761 153765 153767 153769 153770 153771 153773 153774 153775 153777 153779 153783 153785 153789 153791 153795 153801 153803 153809 153813 153815 153819 153825 153831 153833 153839 153843 153845 153851 153855 153861 153869 203614
(1)根据乙醛的结构对性质进行预测
| 乙醛的结构特点 | 可能的化学性质 |
| 有C=O双键,不饱和 | 与H2发生加成反应,乙醛表现氧化性 |
CHO中C-H键极性较强 | CHO中C-H键被氧化,变为C-OH |
(3)设计实验验证乙醛的还原性,请填全表格.
| 实验 | 现象 | 结论 |
| 取适量乙醛溶液,滴加高锰酸钾酸性溶液 | 高锰酸钾溶液紫色变浅(褪去) | 乙醛能被高锰酸钾氧化 |
| 向新制银氨溶液中加入几滴乙醛溶液,水浴加热 | 试管壁上出现银镜(一层光亮如镜的银) | 乙醛将银氨溶液还原 |
| 向新制氢氧化铜悬浊液中加入适量乙醛溶液,加热 | 出现红色沉淀 | 乙醛被氢氧化铜氧化 |
①乙醛被高锰酸钾溶液氧化为CH3COOH(填结构简式)
②写出乙醛发生银镜反应的方程式CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O
(4)某有机物只含C、H、O三种元素,该有机物对氢气的相对密度为15,完全燃烧 0.1mol该有机物生成4.4gCO2和1.8gH2O,该有机物的分子式为CH2O,若红外光谱显示该分子中有醛基,则3g该物质与足量的新制氢氧化铜反应,生成沉淀的质量为28.8g.



 .
. .
. .
.