10.将一小块钠投入含有酚酞的水中,观察现象,并解释(表格可不填满)
| 现象 | 解释 |
| 该反应的化学方程式 | |
9.既能与盐酸反应,又能与NaOH溶液反应的是( )
①Al;②Al(OH)3;③(NH4)2CO3;④Na2CO3;⑤NaHCO3;⑥NaHSO4.
①Al;②Al(OH)3;③(NH4)2CO3;④Na2CO3;⑤NaHCO3;⑥NaHSO4.
| A. | ②③⑤ | B. | ①②③⑤ | C. | ②③④⑤ | D. | ②③④⑤⑥ |
8.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 1mol/L的CaCl2溶液中含Cl-的数目为2NA | |
| B. | 标准状况下,22.4LCl2和H2混合气体原子数为2NA | |
| C. | 0.1mol AlCl3完全转化为氢氧化铝胶体,会生成0.1NA个胶粒 | |
| D. | 常温常压下,100g 40%NaOH水溶液含氧原子总数为NA |
7.有原子序数依次增大的A、B、C、D、E五种短周期元素,它们可两两组成甲、乙、丙、丁四种化合物,各化合物中原子个数比关系如下表:
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多两个;在周期表中,C是E的邻族元素,化学性质活泼;D和E位于同一周期,且D和E的原子序数之和为30.
(1)甲的电子式 ,丁的结构式
,丁的结构式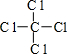
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为 .
.
(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | A:C=1:1 | B:C=1:2 | D:E=1:3 | B:E=1:4 |
(1)甲的电子式
 ,丁的结构式
,丁的结构式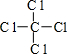
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为
 .
.(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
5.下列各组元素中按微粒半径递增顺序排列的是( )
| A. | Li Na K | B. | Ba2+ Ca2+ Mg2+ | C. | Ca2+ K+ Cl- | D. | N O F |
4.在同温、同压下,相同物质的量的氢气和氦气,具有相同的( )
| A. | 原子数 | B. | 质子数 | C. | 体积 | D. | 质量 |
3.恒温下在密闭容器中进行的反应2SO2+O2?2SO3达到平衡状态的标志是( )
| A. | 容器中SO2、O2、SO3共存 | B. | 容器中SO2 和SO3浓度相同 | ||
| C. | 容器中n(SO2):n(O2):n(SO3)=2:1:2 | D. | 容器中压强不随时间而改变 |
2.下列说法正确的是( )
0 153176 153184 153190 153194 153200 153202 153206 153212 153214 153220 153226 153230 153232 153236 153242 153244 153250 153254 153256 153260 153262 153266 153268 153270 153271 153272 153274 153275 153276 153278 153280 153284 153286 153290 153292 153296 153302 153304 153310 153314 153316 153320 153326 153332 153334 153340 153344 153346 153352 153356 153362 153370 203614
| A. | 在101 kPa时,1 mol H2完全燃烧生成气态水,放出285.8 kJ热量,H2的燃烧热为-285.8 kJ•mol-1 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后终止温度 | |
| C. | 在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ•mol-1 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.31 kJ•mol-1.若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ |