8.下列关于化学平衡的叙述,正确的是( )
| A. | 化学平衡是动态平衡 | |
| B. | 各反应物的浓度等于各生成物的浓度 | |
| C. | 正逆反应速率为零 | |
| D. | 反应物和生成物的浓度不再改变,反应已停止 |
3.A、B、C、D、E是元素周期表中前四周期中五种常见元素,其相关信息如表:
请回答下列问题:
(1)C在元素周期表中位于第三周期、第IA族;D的基态原子核外电子排布式是1s22s22p63s23p4.
(2)B、C、D的简单离子半径由大到小的顺序为(用化学符号表示,下同)S2->O2->Na+,B、D的简单氢化物中稳定性较大的是H2O.
(3)B的常见单质和C的单质按物质的量比1:2反应生成的化合物中化学键的类型为离子键、共价键;该化合物属于离子晶体.
(4)E形成的黑色磁性晶体发生铝热反应的化学方程式是3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3.
(5)已知:2AB(g)+B2(g)═2AB2(g)△H=-566.0kJ•mol-1
D(s)+B2(g)═DB2(g)△H=-296.0kJ•mol-1
处理含AB、DB2烟道气污染的一种方法是将其在催化剂作用下转化为固态单质D,请写出此反应的热化学方程式:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270kJ•mol-1.
| 元素 | 相关信息 |
| A | 原子核外L层电子数是K层的2倍 |
| B | 其一种单质被称为地球生物的“保护伞” |
| C | 元素的第一电离能是第3周期所有元素中最小的 |
| D | 基态原子最外层电子排布为(n+1)sn(n+1)p(n+2) |
| E | 可形成多种氧化物,其中一种为具有磁性的黑色晶体 |
(1)C在元素周期表中位于第三周期、第IA族;D的基态原子核外电子排布式是1s22s22p63s23p4.
(2)B、C、D的简单离子半径由大到小的顺序为(用化学符号表示,下同)S2->O2->Na+,B、D的简单氢化物中稳定性较大的是H2O.
(3)B的常见单质和C的单质按物质的量比1:2反应生成的化合物中化学键的类型为离子键、共价键;该化合物属于离子晶体.
(4)E形成的黑色磁性晶体发生铝热反应的化学方程式是3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3.
(5)已知:2AB(g)+B2(g)═2AB2(g)△H=-566.0kJ•mol-1
D(s)+B2(g)═DB2(g)△H=-296.0kJ•mol-1
处理含AB、DB2烟道气污染的一种方法是将其在催化剂作用下转化为固态单质D,请写出此反应的热化学方程式:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270kJ•mol-1.
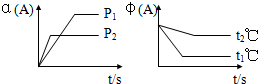
19.一定温度和压强下,下列各可逆反应达到化学平衡状态,各反应有如图所示的对应关系:

(1)N2(g)+3H2(g)?2NH3(g)△H<0(曲线Ⅰ)
(2)H2(g)+I2(g)?2HI(g)△H>0(曲线Ⅱ)
(3)2SO3(g)?2SO2(g)+O2(g)△H>0(曲线Ⅲ)
则下列y轴的表达意义均符合上述三个平衡状态的是( )
0 152409 152417 152423 152427 152433 152435 152439 152445 152447 152453 152459 152463 152465 152469 152475 152477 152483 152487 152489 152493 152495 152499 152501 152503 152504 152505 152507 152508 152509 152511 152513 152517 152519 152523 152525 152529 152535 152537 152543 152547 152549 152553 152559 152565 152567 152573 152577 152579 152585 152589 152595 152603 203614

(1)N2(g)+3H2(g)?2NH3(g)△H<0(曲线Ⅰ)
(2)H2(g)+I2(g)?2HI(g)△H>0(曲线Ⅱ)
(3)2SO3(g)?2SO2(g)+O2(g)△H>0(曲线Ⅲ)
则下列y轴的表达意义均符合上述三个平衡状态的是( )
| A. | 平衡混合气的平均相对分子质量 | |
| B. | 平衡混合气中一种反应物的浓度 | |
| C. | 平衡混合气中一种生成物的体积分数 | |
| D. | 平衡混合气中一种反应物的体积分数 |
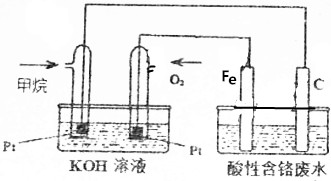

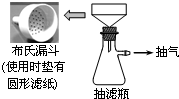 卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定.
卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定. 二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.
二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.