题目内容
20.按要求写热化学方程式:(1)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式NaOH(aq)+$\frac{1}{2}$H2SO4(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
(2)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H=-488.3kJ/mol.
分析 (1)根据中和热的概念:稀的强酸和强碱反应生成1mol水所放出的热量求出中和热以及中和热的热化学方程式;
(2)依据热化学方程式和盖斯定律计算得到所需热化学方程式.
解答 解:(1)1mol H2SO4溶液与足量 NaOH溶液完全反应,放出114.6kJ的热量,即生成2mol水放出114.6kJ的热量,反应的反应热为-114.6kJ/mol,中和热为-57.3kJ/mol,则中和热的热化学方程式:NaOH(aq)+$\frac{1}{2}$H2SO4(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol,
故答案为:NaOH(aq)+$\frac{1}{2}$H2SO4(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol;
(2)①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H=-870.3kJ•mol-1
②C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
依据盖斯定律计算(2)×2+(3)×2-(1)得到C和H2和O2 生成CH3COOH的热化学方程式:
2C(s)+2H2(g)+O2(g)=CH3COOH(l);△H=2×(-393.5kJ/mol)+2×(-285.8kJ/mol)-(-870.3kJ/mol)=-488.3kJ/mol,
所以热化学方程式为2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H=-488.3kJ/mol,
故答案为:2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H=-488.3kJ/mol.
点评 本题考查了热化学方程式的书写方法,主要是燃烧热概念的理解分析,盖斯定律计算应用,键能计算费用焓变的方法,掌握基础是关键,题目较简单.

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案| A. | FeCl3 | B. | Na2CO3 | C. | K2SO3 | D. | TiCl4 |
| A. | C原子的轨道表示式: | |
| B. | N原子轨道表示式: | |
| C. | Cr基态原子核外电子排布式:[Ar]3d54s1 | |
| D. | Ca原子的电子排布式:[Ar]3d2 |
①把盛有溶液的分液漏斗放在铁架台的铁圈中;
②把50mL碘水和15mL CCl4加入分液漏斗中,并盖好玻璃塞;
③检验分液漏斗活塞和上口的玻璃塞是否漏液;
④倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
⑤旋开活塞,用烧杯接收溶液;
⑥从分液漏斗上口倒出上层水溶液;
⑦将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
⑧静置,分层.
正确操作步骤的顺序是( )
| A. | ③②⑧①⑦④⑤⑥ | B. | ③②④①⑦⑧⑤⑥ | C. | ①③④⑦⑧⑤⑥② | D. | ②①③④⑦⑧⑤⑥ |

| A. | 双氢青蒿素属于酯类物质 | |
| B. | 青蒿素的分子式为C15H22O5 | |
| C. | 青蒿素环上的一氢取代物有11种 | |
| D. | 青蒿素通过加成反应可以转化为双氢青蒿素 |
| A. | 乙烯能使酸性高锰酸钾溶液褪色,甲烷则不能使其褪色 | |
| B. | 溶于水能导电的化合物不一定是离子化合物 | |
| C. | 需要加热的反应不一定是吸热反应 | |
| D. | 石油的分馏和煤的干馏都是化学变化 |
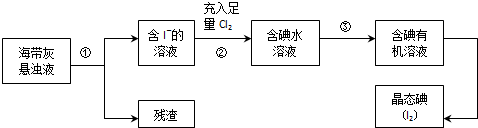
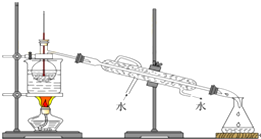
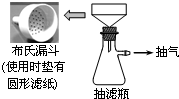 卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定.
卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定.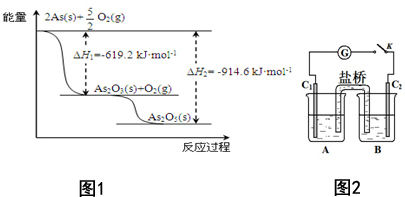 对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.