下表是元素周期表的一部分,请按要求回答有关问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 |
|
|
| ① | ② |
| ③ |
|
3 |
| ④ | ⑤ |
|
| ⑥ | ⑦ | ⑧ |
4 | ⑨ |
|
|
|
|
| ⑩ |
|
(1)表中化学性质最不活泼的元素的原子结构示意图为: ;
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨的最高价氧化物对应的水化物反应的离子方程式: ;
(3)元素④与元素⑦形成的化合物中的化学键类型是 ,写出该化合物的电子式: ;
(4)①②⑥⑦四种元素的最高价氧化物对应的水化物中酸性最弱的是 (填化学式);
(5)元素③与元素⑩两者核电荷数之差是 ;
(6)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的元素是: (填序号);
(7)④⑤⑥⑦四种元素的简单离子的半径由大到小的顺序为: (填化学式).
钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如图(废料中含有Al、Li、Co2O3和Fe2O3等物质).
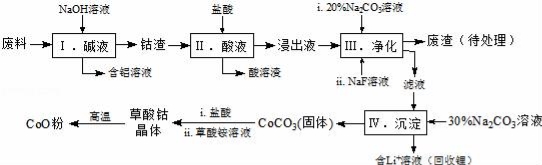
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表.
Fe3+ | Co2+ |
| Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | ﹣0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式: 。
(2)步骤Ⅲ中 Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过 ;废渣中的主要成分除了LiF外,还有 。
(3)NaF 与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是 。
(4)在空气中加热5.49g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表.已知:M(CoC2O4·2H2O)=183g/mol
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
890~ | 2.25 |
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是 。温度高于890℃时,固体产物发生分解反应,固体产物为 。
 B.
B. C.
C.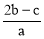 D.
D.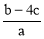
 入pH=11Ba(OH)2溶液,生成BaSO4的质量与加入的Ba(OH)2溶液体积关系如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
入pH=11Ba(OH)2溶液,生成BaSO4的质量与加入的Ba(OH)2溶液体积关系如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算: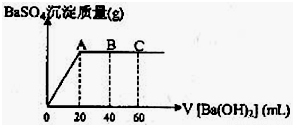
 CaO2·8H2O
CaO2·8H2O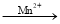 MnO(OH)2
MnO(OH)2 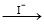 I2
I2 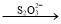 S4O62-
S4O62- 解氧(用mg·L-1表示),写出计算过程。
解氧(用mg·L-1表示),写出计算过程。 Co3+
Co3+ 920
920 量的硫化钠,反应的离子方程式为 。
量的硫化钠,反应的离子方程式为 。