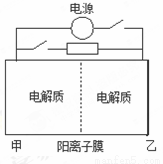
工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g)  Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0
某温度和压强条件下,分别将1.25mol SiCl4(g)、1.0mol N2(g)、10.5mol H2(g)充入20L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是35.0g.已知:
化学键 | Si-Cl | N≡N | H-H | Si-N | H-Cl |
键能(KJ/mol) | a | b | c | d | e |
(1)计算该反应的ΔH=_______________
(2)H2的平均反应速率是
(3)平衡时容器内N2的浓度是
(4)SiCl4(g)的转化率是 %
(5)下图为合成Si3N4反应中SiCl4平衡转化率与温度、压强的关系(n(SiCl4)、n(N2)、n(H2)仍按1.25 mol SiCl4(g)、1.0 mol N2(g)、10.5mol H2(g)投入)
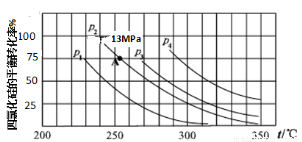
上图中压强最大的是_____(P1、P2、P3、P4),列式计算合成Si3N4反应在图中A点的分压平衡常数Kp= _______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,图中P2=13MPa)
下表为各物质中所含有的少量杂质以及除去这些杂质应选用的试剂或操作方法,正确的一组为
序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
A | C2H5Br | C2H5OH | 用水洗涤、分液 |
B | FeCl3 | CaCO3 | 溶解、过滤、蒸发结晶 |
C | Al2(SO4)3溶液 | MgSO4 | 加入过量烧碱后过滤,再用硫酸酸化滤液 |
D | CO2 | SO2 | 通过盛有品红溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |

 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______。
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______。

 )易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸(
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸( )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)