某温度下,容积同为2L的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知某温度下2HI(g)  H2 (g)+I2 (g) ΔH =+AkJ·mol-1 K=4.0)
H2 (g)+I2 (g) ΔH =+AkJ·mol-1 K=4.0)
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 2 mol HI | 1 mol H2+1 mol I2 | 2 mol HI+1 mol H2 +1 mol I2 |
HI的浓度 | c1 | c2 | c3 |
反应的能量变化 | 吸收akJ | 放出bkJ | 吸收ckJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | a1 | a2 | a3 |
(1)根据上表回答问题
①c1、c3的关系式为 ;②a、b的关系式为 ;
③p2、p3的关系式为 ;④a1与a2的关系式为 ;
(2)甲容器中:该反应的平衡常数表达式为 。
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为 mol·L ·min
·min
(4)丙容器中:反应开始时V正 V逆(填“小于”、“等于”或“大于”)
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气的燃烧热值高,H2(g) +1/2 O2 (g) = H2O (g) ΔH = -241.8 kJ·mol-1
化学键 | H-H | O=O | O-H |
键能(kJ·mol-1) | X | 496.4 | 463 |
请根据相关数据计算:H-H的键能X = ________kJ·mol-1。
(2)根据现代工业技术可以用H2和CO反应来生产燃料甲醇,其反应方程式如下:
CO2 (g) +3H2(g) H2O(l) + CH3OH(g) ΔH = -49.00 kJ·mol-1
H2O(l) + CH3OH(g) ΔH = -49.00 kJ·mol-1
一定温度下,在体积为1 L的密闭容器中充入1.00 mol CO2和3.00 mol H2,测得CO2和CH3OH的浓度随时间变化如图所示。
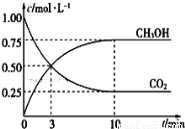
①能说明该反应已达平衡状态的是________(填代号)。
A.CO2在混合气体中的体积分数保持不变
B.单位时间内每消耗1.2 mol H2,同时生成0.4 mol H2O
C.反应中H2O与CH3OH的物质的量浓度比为1:1,且保持不变
②从反应开始到平衡时的平均反应速率v(H2) = ________ ,达到平衡时氢气的转化率为________ 。
③该温度下的平衡常数表达式为________ 。
④下列的条件一定能加快反应速率并且提高H2转化率的是________(填代号)。
A.降低反应温度 B.分离出水
C.保持容器体积不变,充入稀有气体 D.保持容器体积不变,充入CO2气体
 2SO3 ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同的温度下测得气体压强为反应前的92.125%。下列有关叙述正确的是
2SO3 ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同的温度下测得气体压强为反应前的92.125%。下列有关叙述正确的是