0 147199 147207 147213 147217 147223 147225 147229 147235 147237 147243 147249 147253 147255 147259 147265 147267 147273 147277 147279 147283 147285 147289 147291 147293 147294 147295 147297 147298 147299 147301 147303 147307 147309 147313 147315 147319 147325 147327 147333 147337 147339 147343 147349 147355 147357 147363 147367 147369 147375 147379 147385 147393 203614
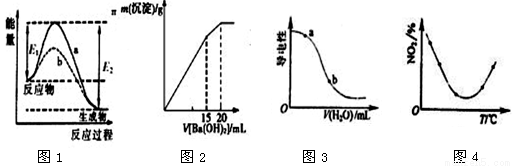
 N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
 用容量瓶配制一定物质的量浓度的溶液,下列操作会使
用容量瓶配制一定物质的量浓度的溶液,下列操作会使 配制的NaOH溶液浓度偏低的是
配制的NaOH溶液浓度偏低的是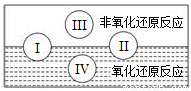
 ═2Ag+O2↑+H2O
═2Ag+O2↑+H2O

 使有效碰撞次数增多
使有效碰撞次数增多