将标准状况下的a L HCl(g)溶于1000g水中,得
到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是( )
A.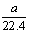 mo1·L-1 B.
mo1·L-1 B.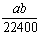 mol·L-1 C.
mol·L-1 C.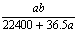 mol·L-1 D.
mol·L-1 D.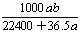 mol·L-1
mol·L-1
下列包装标识贴错了的是( )
| 选项 | A | B | C | D |
| 物质 | 浓硫酸 | 酒精 | 石灰石 | 黑火药 |
| 标识 |
|
|
|
|
 A.碳酸氢铵溶液与过量的氢氧化钠溶液反应 H+ + OH — H2O
A.碳酸氢铵溶液与过量的氢氧化钠溶液反应 H+ + OH — H2O C.钠和冷水反 Na+2H2O N
C.钠和冷水反 Na+2H2O N a++H2↑+OH—
a++H2↑+OH— D.铜片与稀硝酸反应 Cu+NO3—+4H+ Cu2++NO↑+2H2O
D.铜片与稀硝酸反应 Cu+NO3—+4H+ Cu2++NO↑+2H2O




 。
。

 下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( ) ①的步骤中,旋开分液漏斗下端的旋塞,却发现分液漏斗中的液体很难滴下,其原因是 ;
①的步骤中,旋开分液漏斗下端的旋塞,却发现分液漏斗中的液体很难滴下,其原因是 ;