下列各组元素中按微粒半径递增顺序排列的是( )
|
| A. | Li K Na | B. | Ba2+ Ca2+ Mg2+ |
|
| C. | Ca2+ K+ Cl﹣ | D. | N O F |
铜粉放入稀硫酸溶液中,加热后无明显现象发生.当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出.该盐是( )
|
| A. | Fe2(SO4)3 | B. | Na2CO3 | C. | KNO3 | D. | FeSO4 |
下列物质的电子式书写正确的是( )
|
| A. | NaCl | B. | H2S | C. | 氮气 | D. | NH4I |
下列化合物中,既有离子键,又有共价键的是( )
|
| A. | CaO | B. | SiO2 | C. | H2O | D. | Na2O2 |




 D,其结构简式为:
D,其结构简式为: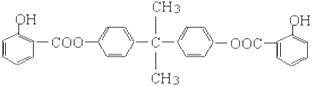

 molNaOH的溶液完全反应。
molNaOH的溶液完全反应。
 阅资料
阅资料 步冷却时间较长,需将溶液置于冷暗处,原因是: 。
步冷却时间较长,需将溶液置于冷暗处,原因是: 。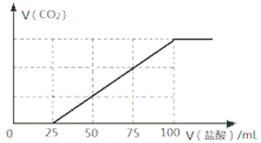
 的量之比为n(NaOH):n(Na2CO3) = 1: 3
的量之比为n(NaOH):n(Na2CO3) = 1: 3