可逆反应:2NO2⇌2NO+O2在固定体积密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2;
②单位时间内生成n mol O2 的同时,生成2n mol NO;
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态;
④混合气体的颜色不再改变的状态;
⑤混合气体的密度不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态.
|
| A. | ①④⑥ | B. | ②③⑤ | C. | ①③④ | D. | ①②③④⑤⑥ |
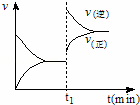
如图为化学反应:4NH3(g)+5O2(g)⇌4NO(g)+6H2O (g);△H<0 在一密闭容器中反应的v﹣t图.下列叙述不符合如图所给信息的是( )
|
| A. | t1时,向容器中通入一定量的NO气体 |
|
| B. | t1时,缩小容器的体积 |
|
| C. | t1时改变外界单一条件时,该反应的平衡常数不一定变化 |
|
| D. | 从t1开始到新的平衡建立的过程中,平衡向逆反应方移动 |
100mL 6mol•L﹣1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量( )
①Na2CO3(s) ②BaCl2(aq) ③Na2S(s) ④CH3COONa(s) ⑤KNO3(aq) ⑥H2O ⑦NaCl(aq)
|
| A. | ①③④⑥ | B. | ②④⑥⑦ | C. | ②③④⑥ | D. | ③④⑤⑦ |
设C+CO2⇌2CO﹣Q1,反应速率v1;N2+3H2⇌2NH3+Q2反应速率v2.对于上述反应,当温度升高时,v1和v2的变化情况为( )
|
| A. | 同时增大 | B. | 同时减小 |
|
| C. | v1增大,v2减小 | D. | v1减小,v2增大 |
有一处于平衡状态的可逆反应:X(s)+3Y(g)⇌2Z(g)(△H<0).为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z.
|
| A. | ①③⑤ | B. | ②③⑤ | C. | ②③⑥ | D. | ②④⑥ |
在一不可变容器中发生如下反应:2NO2(g)⇌2NO(g)+O2(g)△H>0 达到平衡后,升温,混合气体的( )不变.
|
| A. | 密度 | B. | 颜色 | C. | 压强 | D. | 总物质的量 |
下列说法正确的是( )
|
| A. | 增大反应物浓度,可增大活化分子百分数,从而使有效碰撞次数增多 |
|
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 |
|
| C. | 升高温度能使化学反应速率增大的主要原因是增加了反应物分子数 |
|
| D. | 催化剂能增大活化分子百分数,从而成千成万倍地增大化学反应速率 |
